题目内容
某有机物A的质量为64g,在空气中完全燃烧后,只生成88g CO2和72g H2O,试求该化合物中是否有氧元素?该化合物中各元素的质量比是多少?
解:88gCO2中碳元素的质量为88g×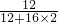 ×100%=24g,
×100%=24g,
72gH2O中氢元素的质量为72g× ×100%=8g,
×100%=8g,
因有机物A燃烧生成二氧化碳和水,
根据质量守恒定律可知元素的质量守恒,
则24g+8g=32g<64g,则说明A中含有氧元素,
氧元素的质量为64g-24g-8g=32g,
则碳、氢、氧元素的质量比为24g:8g:32g=3:1:4,
答:该有机物含有氧元素;碳、氢、氧元素的质量比为3:1:4.
分析:根据二氧化碳和水来计算碳元素和氢元素的质量,若碳和氢元素的质量等于A的质量,则不含氧元素,若小于A的质量,则含有氧元素;利用A的质量减去碳和氢元素的质量即可求氧元素的质量,再计算元素的质量比.
点评:本题考查学生利用质量分数计算化合物中元素的质量,再根据质量守恒定律来分析有机物的组成,学生能利用元素守恒的方法来分析是解答本题的关键.
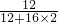 ×100%=24g,
×100%=24g,72gH2O中氢元素的质量为72g×
 ×100%=8g,
×100%=8g,因有机物A燃烧生成二氧化碳和水,
根据质量守恒定律可知元素的质量守恒,
则24g+8g=32g<64g,则说明A中含有氧元素,
氧元素的质量为64g-24g-8g=32g,
则碳、氢、氧元素的质量比为24g:8g:32g=3:1:4,
答:该有机物含有氧元素;碳、氢、氧元素的质量比为3:1:4.
分析:根据二氧化碳和水来计算碳元素和氢元素的质量,若碳和氢元素的质量等于A的质量,则不含氧元素,若小于A的质量,则含有氧元素;利用A的质量减去碳和氢元素的质量即可求氧元素的质量,再计算元素的质量比.
点评:本题考查学生利用质量分数计算化合物中元素的质量,再根据质量守恒定律来分析有机物的组成,学生能利用元素守恒的方法来分析是解答本题的关键.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
 (2012?湛江模拟)湛江廉江盛产红橙,有“中国红橙之乡”之美誉.如右下图:红橙的营养丰富,其果汁中含全糖11.3%,柠檬酸0.85%,维生素C≥30mg/100g.请回答:
(2012?湛江模拟)湛江廉江盛产红橙,有“中国红橙之乡”之美誉.如右下图:红橙的营养丰富,其果汁中含全糖11.3%,柠檬酸0.85%,维生素C≥30mg/100g.请回答: