题目内容
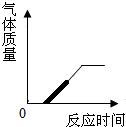
下图为某反应的部分微观示意图,其中不同的球代表不同元素的原子。下列说法正确的是

A.该反应属于化合反应
B.参加反应的两种分子个数比为1∶1
C.各元素的化合价在反应前后未改变
D.1个X分子中有3个原子
【答案】
D
【解析】略

练习册系列答案
相关题目
浩瀚的海洋中蕴藏着丰富的自然资源,现摘取部分海水综合利用的方案如下:
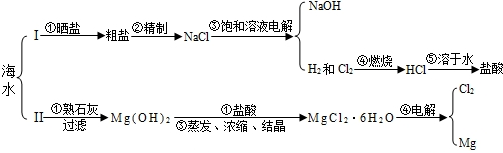
请根据下列部分酸碱盐溶解性表回答下列问题:
(1)除去粗盐中混有的少量不溶性杂质,下列操作顺序正确的是 (填编号,下同)
①过滤 ②溶解 ③蒸发
(2)过滤后所得滤液仍然浑浊,可能的原因是 ;
①滤纸破损 ②过滤时漏斗里的液面高于滤纸的边缘 ③漏斗颈下端管口没有紧靠烧杯内壁.
(3)如果海水中含有的可溶性杂质主要为CaCl2、MgSO4,则方案Ⅰ中步骤②“精制”时:欲沉淀杂质CaCl2,一般加入稍过量的碳酸钠溶液,此反应方程式为 ;
如果井水或溪水中含有Ca2+、Mg2+,这种水称作 ,如果在这种水中加入肥皂,会出现 .
(4)方案Ⅱ中步骤①生成Mg(OH)2的反应方程式为 ;
如果熟石灰是用海边的贝壳(主要成分为CaCO3)生成的,则生产熟石灰的反应方程式为: 、 .
(5)方案Ⅱ中除步骤①中用过滤外,还要用到“过滤”步骤的是 (填序号).
(6)下图是某种加钙食盐包装袋标签上的部分说明文字(Ca-40,C-12,O-16):
如果每袋加钙食盐含Ca为0.5%,则含CaCO3的质量为 g.
(7)某化工厂为测定氯化钠样品的纯度,取30g氯化钠样品(杂质为氯化钙)溶于水制成252g溶液,再加入53g溶质质量分数为10%的碳酸钠溶液,恰好完全反应.求:
①样品中杂质CaCl2的质量;
②样品中氯化钠的质量;
③样品中氯化钠的质量分数;
④反应后所得溶液中溶质的质量分数.

请根据下列部分酸碱盐溶解性表回答下列问题:
| OH- | Cl- | SO42- | CO32- | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 微 | 不 |
| Ba2+ | 溶 | 溶 | 不 | 不 |
| Mg2+ | 不 | 溶 | 溶 | 不 |
①过滤 ②溶解 ③蒸发
(2)过滤后所得滤液仍然浑浊,可能的原因是
①滤纸破损 ②过滤时漏斗里的液面高于滤纸的边缘 ③漏斗颈下端管口没有紧靠烧杯内壁.
(3)如果海水中含有的可溶性杂质主要为CaCl2、MgSO4,则方案Ⅰ中步骤②“精制”时:欲沉淀杂质CaCl2,一般加入稍过量的碳酸钠溶液,此反应方程式为
如果井水或溪水中含有Ca2+、Mg2+,这种水称作
(4)方案Ⅱ中步骤①生成Mg(OH)2的反应方程式为
如果熟石灰是用海边的贝壳(主要成分为CaCO3)生成的,则生产熟石灰的反应方程式为:
(5)方案Ⅱ中除步骤①中用过滤外,还要用到“过滤”步骤的是
(6)下图是某种加钙食盐包装袋标签上的部分说明文字(Ca-40,C-12,O-16):
| 配料表:氯化钠、食用碳酸钙、碘酸钾 净含量:500g 成分表:氯化钠≥88% 钙(以Ca计)(0.5-1.3)% 碘(以I计)(20-50)mg/kg |
(7)某化工厂为测定氯化钠样品的纯度,取30g氯化钠样品(杂质为氯化钙)溶于水制成252g溶液,再加入53g溶质质量分数为10%的碳酸钠溶液,恰好完全反应.求:
①样品中杂质CaCl2的质量;
②样品中氯化钠的质量;
③样品中氯化钠的质量分数;
④反应后所得溶液中溶质的质量分数.
(1)酸、碱、盐溶解性表是学习化学的重要工具.右表列出了“部分酸、碱、盐在20℃时的溶解性”.请按下列要求填写有关内容:
判断:NaNO3与BaCl2溶液能否发生反应?
填“是”或“否”);理由是 ;
写出铁或铝与表中的一种盐反应的化学方程式:
(2)浓硫酸和稀硫酸,在实验室中敞口放置,它们的质量和放置天数的关系如下图.
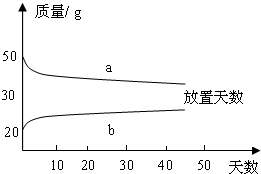
a、b曲线中表示浓硫酸的是(填字母序号) ;理由是 .
(3)①某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸.若要清洗100kg的这种石油产品,理论上需要NaOH kg.
②石化厂进行了技术改造,改用Ca(OH)2中和这些残余硫酸.每处理100kg这种产品,可以节约多少经费?( NaOH和Ca(OH)2的市场价格如下表):
| OH- | NO3- | Cl- | CO32- | SO42- | |
| H+ | 溶、挥 | 溶、挥 | 溶、挥 | 溶 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ca+ | 微 | 溶 | 溶 | 不 | 微 |
| Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
| Cu2+ | 不 | 溶 | 溶 | 不 | 溶 |
写出铁或铝与表中的一种盐反应的化学方程式:
(2)浓硫酸和稀硫酸,在实验室中敞口放置,它们的质量和放置天数的关系如下图.

a、b曲线中表示浓硫酸的是(填字母序号)
(3)①某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸.若要清洗100kg的这种石油产品,理论上需要NaOH
②石化厂进行了技术改造,改用Ca(OH)2中和这些残余硫酸.每处理100kg这种产品,可以节约多少经费?( NaOH和Ca(OH)2的市场价格如下表):
| 名称 | NaOH | Ca(OH)2 |
| 价格(元/kg) | 20.00 | 6.00 |
 13、有A、B、C、D、E、F六种物质的稀溶液,已知它们分别是K2CO3、BaCl2、Ca(NO3)2、NaCl、H2SO4、AgNO3中的某一种溶液.下图为常温时上述溶液两两混合的部分实验现象,其中“↓”表示生成沉淀,“↑”表示生成气体,“-”表示无明显现象或生成微溶物.请回答下列问题:
13、有A、B、C、D、E、F六种物质的稀溶液,已知它们分别是K2CO3、BaCl2、Ca(NO3)2、NaCl、H2SO4、AgNO3中的某一种溶液.下图为常温时上述溶液两两混合的部分实验现象,其中“↓”表示生成沉淀,“↑”表示生成气体,“-”表示无明显现象或生成微溶物.请回答下列问题: