题目内容
4. 现有50gHCl和CuCl2的混合溶液,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图所示.请回答下列问题:
现有50gHCl和CuCl2的混合溶液,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成沉淀的质量与加入NaOH溶液的质量关系如图所示.请回答下列问题:(1)当加入NaOH溶液的质量为a g时,溶液中的溶质是NaCl、NaOH.
(2)求混合溶液中CuCl2的质量分数.
分析 (1)根据氢氧化钠与盐酸反应生成氯化钠和水,氢氧化钠与氯化铜反应生成氢氧化铜沉淀和氯化钠,还需要结合a点时氢氧化钠过量进行分析;
(2)氢氧化钠与氯化铜反应生成氢氧化铜沉淀和氯化钠,根据沉淀的质量计算出氯化铜的质量,再用氯化铜的质量除以50g即可.
解答 解:(1)向50gHCl和CuCl2的混合溶液中逐滴加入溶质质量分数为10%的NaOH溶液,氢氧化钠先与盐酸反应生成氯化钠和水,当盐酸反应完成后氢氧化钠与氯化铜反应生成氢氧化铜沉淀和氯化钠,所以反应后溶液中的溶质一定含有氯化钠,a点时氢氧化钠过量,所以溶质中还含有氢氧化钠;
(2)设混合溶液中CuCl2的质量为x.
CuCl2+2NaOH=Cu(OH)2↓+2NaCl
135 98
x 9.8 g
$\frac{135}{98}=\frac{x}{9.8g}$ 解得:x=13.5 g
混合溶液中CuCl2的质量分数=$\frac{13.5g}{50g}×100%$=27%.
故答为:(1)NaCl、NaOH.(2)求混合溶液中CuCl2的质量分数是27%.
点评 本题考查化学方程式与溶液的综合计算,解题关键是分析清楚反应过程的先后,找出每个过程中已知物质的质量.要知道加入的氢氧化钠先与盐酸反应,把盐酸反应完了再与氯化铜反应.

练习册系列答案
相关题目
11.化学概念在逻辑上存在如图所示关系,对下列概念间的关系说法正确的是( )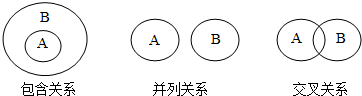
①纯净物与混合物属于包含关系
②化合物与氧化物属于包含关系
③单质与化合物属于交叉关系
④金属元素与非金属元素属于并列关系
⑤中和反应与复分解反应属于并列关系
⑥有机化合物与无机化合物属于并列关系.

①纯净物与混合物属于包含关系
②化合物与氧化物属于包含关系
③单质与化合物属于交叉关系
④金属元素与非金属元素属于并列关系
⑤中和反应与复分解反应属于并列关系
⑥有机化合物与无机化合物属于并列关系.
| A. | ①③ | B. | ②④⑥ | C. | ③⑤ | D. | ①③⑤ |
12.下列图象能正确表示对应变化关系的是( )
| A. |  表示水通电分解产生的气体质量m与反应时间t的关系 | |
| B. |  表示两份完全相同的双氧水在有无MnO2的情况下,产生的O2的质量与反应时间t的关系 | |
| C. |  表示往锌中加入足量的稀H2SO4,产生的H2的质量m与反应时间t的关系 | |
| D. |  用水稀释pH=10的溶液 |
19.将一根洁净的铁钉放入一定质量的稀硫酸中,充分反应后,所得溶液中的溶质是( )
| A. | 铁钉 | |
| B. | 硫酸 | |
| C. | 一定是硫酸亚铁 | |
| D. | 可能是硫酸亚铁,也可能是硫酸和硫酸亚铁 |
14.在一定温度下,食盐的饱和溶液一定是( )
| A. | 很浓的溶液 | B. | 不能继续溶解氯化钠的溶液 | ||
| C. | 很稀的溶液 | D. | 不能继续溶解其他物质的溶液 |
 2013年12月2日,我国在西昌成功发射“嫦娥三号”卫星.“嫦娥三号”是我国国家航天局嫦娥工程第二阶段的登月探测器,由着陆器和巡视探测器(即“玉兔号”月球车)组成,进行首次月球软着陆和自动巡视勘察,获取月球内部的物质成分并进行分析,将一期工程的“表面探测”引申内部探测.月球上像沙子样的月壤颗粒对月球车磨损非常厉害,所以制作月球车的材料必须具备性质(答出三点).
2013年12月2日,我国在西昌成功发射“嫦娥三号”卫星.“嫦娥三号”是我国国家航天局嫦娥工程第二阶段的登月探测器,由着陆器和巡视探测器(即“玉兔号”月球车)组成,进行首次月球软着陆和自动巡视勘察,获取月球内部的物质成分并进行分析,将一期工程的“表面探测”引申内部探测.月球上像沙子样的月壤颗粒对月球车磨损非常厉害,所以制作月球车的材料必须具备性质(答出三点).