题目内容
3.相同质量的镁、铝、锌、铁,分别跟足量的相同浓度的稀盐酸反应,反应情况用如图图线表示,纵坐标是氢气的质量,横坐标是反应时间,其中图线正确的是( )| A. |  | B. |  | C. |  | D. |  |
分析 根据在金属活动性顺序中,镁>铝>锌>铁,金属的位置越靠前,与酸反应生成氢气的速度越快,在坐标中表现曲线越陡,相同质量的镁、铝、锌、铁分别和足量的稀盐酸反应,铝产生的氢气量多,锌产生的氢气最少进行分析.
解答 解:根据金属活动性顺序的意义,金属的位置越靠前,与酸反应生成氢气的速度越快,在坐标中表现曲线越陡,相同质量的镁、铝、锌、铁分别和足量的稀盐酸反应,铝产生的氢气量多,锌产生的氢气最少.观察反应图象,
A、镁生成的氢气不会比铝多,故A错误;
B、铝的反应速率不会比镁快,故B错误;
C、铁的反应速率不会比锌快,故C错误;
D、根据图象,铝产生的氢气比锌多,锌产生的氢气最少,镁速度最块,铝速度比锌快,符合题意,故D正确.
故选:D.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序的意义进行.

练习册系列答案
相关题目
13.下列实验方案,不能达到预期目的是( )
| A. | 用体温计测量人体的温度 | |
| B. | 用测电笔辨别火线和零线 | |
| C. | 用排水集气法收集氧气 | |
| D. | 用酚酞试液鉴别稀硫酸和硫酸钠溶液 |
14.下列实验操作中正确的是( )
| A. | 给试管中的液体加热,试管中的液体体积一般不超过试管容积的$\frac{1}{2}$ | |
| B. | 取液后的滴管不能倒置,但可平放 | |
| C. | 在无药量说明的情况下,某同学取用稀硫酸时,量取了2毫升 | |
| D. | 若取用的药品没有腐蚀性(如铁钉)可以用手拿 |
8.下列各项中,不属于我国《环境空气质量标准》基本监控项目的是( )
| A. | 二氧化硫 | B. | 氮气 | C. | 二氧化氮 | D. | PM2.5 |
12.有40g5%的氯化钾溶液,若将其溶质的质量分数增大到10%,应采用的方法是( )
| A. | 把溶剂蒸发掉一半 | B. | 加入40g15%的氯化钠溶液 | ||
| C. | 把溶剂蒸发掉20g | D. | 加入2g氯化钾晶体 |
13.除去CO2中混有少量的CO,得到较纯净的CO2,应采用有效方法是( )
| A. | 将混合气体通入澄清石灰水 | |
| B. | 将混合气体通过灼热的氧化铜层 | |
| C. | 将混合气体点燃,使一氧化碳燃烧 | |
| D. | 将集气瓶口朝上,移开玻璃片使一氧化碳逸出 |
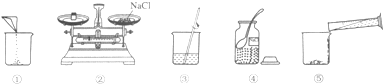 如图是配置氯化钠溶液的实验操作:
如图是配置氯化钠溶液的实验操作: