题目内容
根据质量守恒定律,2g氢气和8g氧气充分燃烧可生成水( )
| A、10g | B、9g | C、8.5g | D、条件不足,无法确定 |
分析:根据题干信息可知,氢气燃烧时会生成水.由它们反应的化学方程式各种物质的比例关系应用于质量守恒定律分析.
解答:解:由化学方程式2H2+O2
2H2O能够可知:每有4份质量的氢气和32份质量的氧气在点燃的条件下完全化合生成36份质量的水,即参加反应的氢气、氧气和生成的二氧化碳质量之比=1:8:9,因此1g氢气与8g氧气反应生成9g水,1g氢气剩余.
故选:B.
| ||
故选:B.
点评:化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和即质量守恒定律.在这里要注意“参加反应”这四个字的含义.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
在实验室制取氧气时,取MnO2和KClO3的固体混合物15.25g,加热至不再产生气体为止,收集到一定质量的氧气.某化学兴趣小组欲求得所制氧气的质量,他们将加热后剩余物冷却到一定温度后,通过多次加水测定剩余物质量的办法即可求出.加水的质量与剩余固体的质量见下表:(MnO2是不溶于水的固体粉末)
试求:(2KClO3-245,O2-32)
(1)写出氯酸钾、二氧化锰混合加热的化学方程式: ;
(2)加热t3时间后,小明认为氯酸钾已经完全反应,请你帮他说明理由? ;
(3)小华根据质量守恒定律很快得到O2的质量是 g;
(4)请你通过计算,帮助他们说明该药品氯酸钾是否纯净.
| 编号 | 1 | 2 | 3 | 4 |
| 加水的质量(g) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 7.25 | 4.05 | m | 3 |
(1)写出氯酸钾、二氧化锰混合加热的化学方程式:
(2)加热t3时间后,小明认为氯酸钾已经完全反应,请你帮他说明理由?
(3)小华根据质量守恒定律很快得到O2的质量是
(4)请你通过计算,帮助他们说明该药品氯酸钾是否纯净.
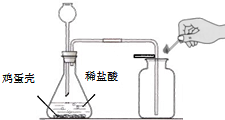 (2010?松江区一模)小张同学为了测定鸡蛋壳中碳酸钙的质量分数,进行了如下实验探究.
(2010?松江区一模)小张同学为了测定鸡蛋壳中碳酸钙的质量分数,进行了如下实验探究.