题目内容
烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g。某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量记录如下:
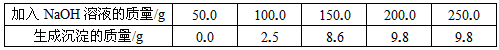
(1)得到沉淀的总质量为??????????????? g,该混合溶液中硫酸铜的质量为????????????????? g。
(2)参加反应的NaOH溶液的总质量是多少克?(要求写出计算过程)
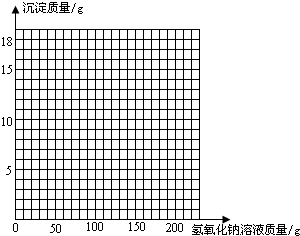
(3)画出在该混合溶液中加入NaOH溶液质量与生成沉淀质量变化关系的曲线。
(1)9.8?? 16.0?? (2)160
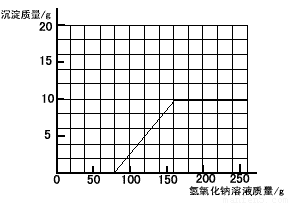
(3)
【解析】
试题分析:(1)据上表记录的数据可知,刚开始加入NaOH溶液,并没有生成沉淀,原因是原烧杯中装有一定量硫酸和硫酸铜的混合溶液,加入的NaOH溶液是先和硫酸反应:H2SO4 + 2NaOH=Na2SO4 + 2H2O,然后随着NaOH溶液的不断加入,过量的NaOH溶液与硫酸铜反应生成沉淀:2NaOH + CuSO4=Cu(OH)2↓ + Na2SO4
,所以随着NaOH溶液的继续加入,生成的沉淀质量也就越来越大,最终保持9.8g不变,表示反应结束,硫酸铜被消耗完,根据硫酸铜和沉淀Cu(OH)2的质量关系,即可算出硫酸铜的质量
(2)同样,化学反应:2NaOH + CuSO4=Cu(OH)2↓ + Na2SO4中,根据NaOH与沉淀Cu(OH)2的质量关系,也可算出参加反应的NaOH溶质的质量,题目已知NaOH溶液的溶质质量分数,这样就可以求出参加反应的NaOH溶液的总质量
(3)画图象,一定要注意两个点:起始点(表示某反应的开始)、转折点(表示某反应的结束),正如刚才分析的,刚开始加入NaOH溶液,并没有生成沉淀,原因是原烧杯中装有一定量硫酸和硫酸铜的混合溶液,加入的NaOH溶液是先和硫酸反应:H2SO4 + 2NaOH=Na2SO4 + 2H2O,而原溶液中含H2SO4的质量为9.8g,根据化学方程式中NaOH和H2SO4的质量关系,即可算出要把9.8g H2SO4完全反应掉需要的NaOH质量,这也就是图象中的起始点,而反应结束时消耗的NaOH质量,在第(2)问已经求出,即图象中的转折点,这时溶液中硫酸铜也被全部消耗,所以沉淀质量也就不再发生变化
(2)解:设与硫酸反应的NaOH的质量为x ,与CuSO4反应的NaOH的质量为y。
H2SO4+ 2NaOH=Na2SO4 + 2H2O CuSO4 + 2NaOH =Cu(OH)2↓+ Na2SO4
98???? 80 ????????????????????????? 80 ??? 98?
9.8g?? x ?????????????????????????? y ???? 9.8g?????
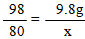 ?????????????????????????
????????????????????????? 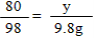
x = 8g???????????????????????????????????? y =8g
故参加反应的NaOH溶液的质量共为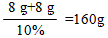
答:整个过程中参加反应的NaOH溶液的总质量是160克。
考点:根据化学方程式进行计算

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| 加入NaOH溶液的质量/g | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| 生成沉淀的质量/g | 0.0 | 2.5 | 8.6 | 9.8 | 9.8 |
(2)参加反应的NaOH溶液的总质量是多少克?(要求写出计算过程)
(3)画出在该混合溶液中加入NaOH溶液质量与生成沉淀质量变化关系的曲线(见答题卡).
| 加入NaOH溶液的质量/g | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| 生成沉淀的质量/g | 0.0 | 2.45 | 8.6 | 9.8 | 9.8 |
(2)参加反应的NaOH溶液的总质量是多少克?(要求写出计算过程)