题目内容
16.黄铜是Zn以主要添加元素的铜合金.黄铜渣中约含Zn 7%、ZnO 31%、Cu 50%、CuO 5%,其余为杂质.处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水、不参与反应):
(1)溶液A中的金属阳离子有Zn2+、Cu2+(填化学式)
(2)溶液A小于(填“大于”、“小于”或“等于”)溶液C的质量.
分析 (1)根据锌、氧化锌、氧化铜与稀硫酸反应的产物来分析;
(2)根据反应的化学方程式的质量关系来分析.
解答 解:(1)锌与稀硫酸反应生成硫酸锌和氢气,氧化锌与硫酸反应生成硫酸锌和水,氧化铜与硫酸反应生成硫酸铜和水,其中的金属阳离子是锌离子和铜离子;
故填:Zn2+、Cu2+;
(2)A到C的过程中发生的反应是:Zn+CuSO4=Cu+ZnSO4,
160 161
由此可见,锌置换出了溶液中的铜,溶液的质量增重了.
故填:小于.
点评 本题重点考查了金属活动性顺序及其应用,了解相关知识即可正确解答,能够考查学生的分析问题能力.

练习册系列答案
相关题目
6.下列化肥属于复合肥的是( )
| A. | (NH4)3PO4 | B. | Ca(H2PO4)2 | C. | CO(NH2)2 | D. | NH4HCO3 |
7. 某同学向如图实验装置中通入气体X,若关闭活塞A,澄清石灰水变浑浊;若打开活塞A,澄清石灰水不变浑浊.则气体X和洗气瓶内溶液Y分别可能是( )
某同学向如图实验装置中通入气体X,若关闭活塞A,澄清石灰水变浑浊;若打开活塞A,澄清石灰水不变浑浊.则气体X和洗气瓶内溶液Y分别可能是( )
 某同学向如图实验装置中通入气体X,若关闭活塞A,澄清石灰水变浑浊;若打开活塞A,澄清石灰水不变浑浊.则气体X和洗气瓶内溶液Y分别可能是( )
某同学向如图实验装置中通入气体X,若关闭活塞A,澄清石灰水变浑浊;若打开活塞A,澄清石灰水不变浑浊.则气体X和洗气瓶内溶液Y分别可能是( )| A | B | C | D | |
| X | CO2 | HCl | CO2 | HCl |
| Y | NaOH | 浓硫酸 | 浓硫酸 | Na2CO3 |
| A. | X:CO2、Y:NaOH | B. | X:HCl、Y:浓硫酸 | C. | X:CO2、Y:浓硫酸 | D. | X:HCl、Y:Na2CO3 |
8.一个C60分子由60个相同的碳原子构成,形似足球,又名足球烯.由C60分子构成的物质属于( ) 

| A. | 单质 | B. | 氧化物 | C. | 有机物 | D. | 化合物 |
16.甲、乙两种固体物质的溶解度曲线如图所示.下列叙述正确的是( )
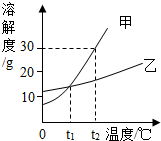

| A. | t1℃时,甲和乙溶液中溶质的质量分数一定相等 | |
| B. | t2℃时,用等质量的甲和乙固体配制饱和溶液,得到乙溶液的质量大于甲 | |
| C. | 将t1℃时的甲、乙饱和溶液升温至t2℃,甲溶液中溶质的质量分数会比乙大 | |
| D. | 用升温的方法能使甲的不饱和溶液变成饱和溶液 |
 某同学用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na 2CO 3溶液,他决定利用该溶液,测定Na 2CO 3溶液中溶质的质量分数.他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na 2CO 3溶液的质量与生成沉淀质量的关系如图所示.
某同学用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na 2CO 3溶液,他决定利用该溶液,测定Na 2CO 3溶液中溶质的质量分数.他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na 2CO 3溶液的质量与生成沉淀质量的关系如图所示. 
 5月18日,我国在南海进行的“可燃冰”试采获得成功.在由烟台建造的半潜式钻井平台“蓝鲸1号”上,通过对海底可燃冰矿藏进行降压使可燃冰分解,再通过沙、水、气分离技术获得连续稳定的天然气.
5月18日,我国在南海进行的“可燃冰”试采获得成功.在由烟台建造的半潜式钻井平台“蓝鲸1号”上,通过对海底可燃冰矿藏进行降压使可燃冰分解,再通过沙、水、气分离技术获得连续稳定的天然气.