题目内容
(2013?济宁)一包白色粉末由硫酸铜、碳酸钙、氯化钡、硫酸钠、氢氧化钠中的三种混合而成,为探究其组成,进行以下实验:
分析实验过程,回答;
(1)白色粉末中一定有
(2)白色粉末的三种成分的可能组合为
分析实验过程,回答;
(1)白色粉末中一定有
碳酸钙、氢氧化钠
碳酸钙、氢氧化钠
,一定没有硫酸铜
硫酸铜
;(2)白色粉末的三种成分的可能组合为
碳酸钙、氢氧化钠、氯化钡
碳酸钙、氢氧化钠、氯化钡
,碳酸钙、氢氧化钠、硫酸钠
碳酸钙、氢氧化钠、硫酸钠
.
分析:由于白色粉末溶于水后能得到沉淀和溶液,溶液为无色,所以固体中一定不会含有硫酸铜,沉淀是原来具有的不溶物碳酸钙或硫酸钠和氯化钡反应生成的硫酸钡沉淀,而该沉淀能够溶于盐酸且生成气体,所以该沉淀不可能是硫酸钡,则一定是碳酸钙,溶于水后的溶液pH大于7,所以溶液显碱性,则固体中一定含有氢氧化钠,据此分析解答即可;
解答:解:由于白色粉末溶于水后能得到沉淀和溶液,溶液为无色,所以固体中一定不会含有硫酸铜,沉淀是原来具有的不溶物碳酸钙或硫酸钠和氯化钡反应生成的硫酸钡沉淀,而该沉淀能够溶于盐酸且生成气体,所以该沉淀不可能是硫酸钡,则一定是碳酸钙,溶于水后的溶液pH大于7,所以溶液显碱性,则固体中一定含有氢氧化钠;
(1)由分析知固体中一定含有碳酸钙和氢氧化钠,一定没有硫酸铜;
(2)由于固体中含有三种物质,而氯化钡、硫酸钠不能同时具有,所以白色粉末的三种成分的可能组合为:碳酸钙、氢氧化钠、氯化钡;碳酸钙、氢氧化钠、硫酸钠;
故答案为:(1)碳酸钙、氢氧化钠;硫酸铜;(2)碳酸钙、氢氧化钠、氯化钡;碳酸钙、氢氧化钠、硫酸钠;
(1)由分析知固体中一定含有碳酸钙和氢氧化钠,一定没有硫酸铜;
(2)由于固体中含有三种物质,而氯化钡、硫酸钠不能同时具有,所以白色粉末的三种成分的可能组合为:碳酸钙、氢氧化钠、氯化钡;碳酸钙、氢氧化钠、硫酸钠;
故答案为:(1)碳酸钙、氢氧化钠;硫酸铜;(2)碳酸钙、氢氧化钠、氯化钡;碳酸钙、氢氧化钠、硫酸钠;
点评:解答本题要掌握各种物质的性质和过程中的实验现象等方面的知识,只有这样才能对问题做出正确的判断;

练习册系列答案
相关题目
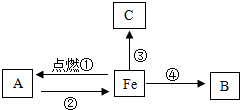 (2013?济宁模拟)构建知识网络是一种重要的学习方法.如图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为红色固体单质.请回答下列问题:
(2013?济宁模拟)构建知识网络是一种重要的学习方法.如图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为红色固体单质.请回答下列问题: (2013?济宁模拟)现有含杂质的氧化铁样品(杂质不参加反应),为了测定该样品中氧化铁的质量分数,某同学称取样品10克,并用如图所示装置进行实验,得到以下两组实验数据.
(2013?济宁模拟)现有含杂质的氧化铁样品(杂质不参加反应),为了测定该样品中氧化铁的质量分数,某同学称取样品10克,并用如图所示装置进行实验,得到以下两组实验数据.