题目内容
12. 如图所示为向一定量某固体中逐滴加入某溶液至过量.若x轴表示加入溶液的质量,则y轴表示的含义是( )
如图所示为向一定量某固体中逐滴加入某溶液至过量.若x轴表示加入溶液的质量,则y轴表示的含义是( )| 选项 | 固体 | 溶液 | Y轴含义 |
| A | 氢氧化铜 | 盐酸 | 水的质量 |
| B | 大理石(杂质不反应) | 稀盐酸 | 溶液中氯化钙的质量分数 |
| C | 铁粉和铜粉的混合物 | 硫酸铜溶液 | 混合物中的铜的质量 |
| D | 氢氧化钠和碳酸钠的混合物 | 稀硫酸 | 二氧化碳的体积 |
| A. | A | B. | B | C. | C | D. | D |
分析 可以根据具体的反应,结合图象完成本题.
A、氢氧化铜固体中开始不含有水;
B、大理石中含有碳酸钙和杂质与稀盐酸反应,碳酸钙被消耗减少,而溶液中氯化钙的质量分数从0开始,不断增加;
C、铁与硫酸铜溶液反应,导致混合物中铜的质量,会不断增加,反应完则质量不变;
D、氢氧化钠和碳酸钠的混合物中开始时没有二氧化碳.
解答 解:A、氢氧化铜固体中开始不含有水,不会出现不变的情况,故A错误;
B、向大理石中加入稀盐酸,会反应生成二氧化碳气体,随着反应的进行,碳酸钙不断被消耗,而溶液中氯化钙的质量分数从0开始,不断增加,故B错误;
C、向铁粉和铜粉的混合物中加入硫酸铜溶液,开始时铁与硫酸铜溶液反应,导致混合物中铜的质量,会不断增加,反应完则质量不变,故C正确;
D、向氢氧化钠和碳酸钠钠的混合物中加入盐酸,会产生二氧化碳气体,但是开始时并没有二氧化碳,故D错误,
故选:C.
点评 本题考查了常见物质间的反应,完成此题,可以根据具体的反应结合图象进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列叙述正确的是( )
| A. | 水结冰后分子停止运动 | |
| B. | 氯化钠晶体由氯化钠分子构成 | |
| C. | 氢原子和氯原子保持氯化氢的化学性质 | |
| D. | 原子和离子都可以构成物质 |
3. 镁将成为2 1世纪重要的轻型环保材料,我国含有非常丰富的镁资源.老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属.但拿出的镁条总是有一层灰黑色的“外衣“,这层灰黑色的外衣是什么物质呢?
镁将成为2 1世纪重要的轻型环保材料,我国含有非常丰富的镁资源.老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属.但拿出的镁条总是有一层灰黑色的“外衣“,这层灰黑色的外衣是什么物质呢?
猜想:小明认为可能是MgO;
小赵认为可能是Mg2(OH)2C03;
小花认为可能是Mg(OH)2.
小赵认为小明的猜想是错误的,其理由是氧化镁通常为白色固体.
实验探究:小赵按图所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体.
实验分析:实验后,小赵认为小花的猜测也是错误的,其理由是石灰水变浑浊的现象可说明此变化过程中有二氧化碳生成,而氢氧化镁中根本不含碳元素.
查阅资料得出结论:Mg(O H)2和Mg2(OH)2C03都可以加热分解,产物均为氧化物,据此请你写出Mg2(OH)2C03加热分解的化学方程式Mg2(OH)2C03$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+H2O+CO2↑
(3)已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为证明Al、Fe和Cu的存在并测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究.
资料在线:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH═2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
①化学兴趣小组的同学讨论了证明金属粉末中存在Al、Fe和Cu的实验设计,下列他们的说法正确的是AB.
A.先加氢氧化钠溶液后加稀盐酸 B.加入的溶液都要过量
C.反应过程中溶液始终是无色 D.充分反应到最后,无固体残留
 ②为探究该金属粉末中Al的质量分数,取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如图:
②为探究该金属粉末中Al的质量分数,取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如图:
I.分析以上数据可知,上表中n的值为14.6;
加入NaOH溶液的质量/g
II.该金属粉末中Al的质量分数为70%%
III.列式计算:第一次参加反应氢氧化钠的质量?
 镁将成为2 1世纪重要的轻型环保材料,我国含有非常丰富的镁资源.老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属.但拿出的镁条总是有一层灰黑色的“外衣“,这层灰黑色的外衣是什么物质呢?
镁将成为2 1世纪重要的轻型环保材料,我国含有非常丰富的镁资源.老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属.但拿出的镁条总是有一层灰黑色的“外衣“,这层灰黑色的外衣是什么物质呢?猜想:小明认为可能是MgO;
小赵认为可能是Mg2(OH)2C03;
小花认为可能是Mg(OH)2.
小赵认为小明的猜想是错误的,其理由是氧化镁通常为白色固体.
实验探究:小赵按图所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体.
实验分析:实验后,小赵认为小花的猜测也是错误的,其理由是石灰水变浑浊的现象可说明此变化过程中有二氧化碳生成,而氢氧化镁中根本不含碳元素.
查阅资料得出结论:Mg(O H)2和Mg2(OH)2C03都可以加热分解,产物均为氧化物,据此请你写出Mg2(OH)2C03加热分解的化学方程式Mg2(OH)2C03$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+H2O+CO2↑
(3)已知某金属粉末中除含有Al外还含有一定量的Fe和Cu,为证明Al、Fe和Cu的存在并测定其中Al的质量分数,某化学兴趣小组的同学展开了如下的实验探究.
资料在线:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH═2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
①化学兴趣小组的同学讨论了证明金属粉末中存在Al、Fe和Cu的实验设计,下列他们的说法正确的是AB.
A.先加氢氧化钠溶液后加稀盐酸 B.加入的溶液都要过量
C.反应过程中溶液始终是无色 D.充分反应到最后,无固体残留
| 加NaOH溶液的次数 | 第一次 | 第二次 | 第三次 | … |
| 剩余固体的质量/g | 1 7.3 | n | 11.9 | … |
 ②为探究该金属粉末中Al的质量分数,取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如图:
②为探究该金属粉末中Al的质量分数,取20g该金属粉末,把100g氢氧化钠溶液平均分成5份依次加入,充分反应后,过滤出固体,将其洗涤、干燥、称量.实验过程中得到的部分数据与图象如图:I.分析以上数据可知,上表中n的值为14.6;
加入NaOH溶液的质量/g
II.该金属粉末中Al的质量分数为70%%
III.列式计算:第一次参加反应氢氧化钠的质量?
20.下列溶液暴露在空气中,质量不变的是( )
| A. | 浓盐酸 | B. | 能硫酸 | C. | 生石灰 | D. | 氯化钠 |
4.我国新修订的《环境空气质量标准》颁布后,各地采取多种措施提高空气质量.下列措施中,不利于提高空气质量的是( )
| A. | 向煤炭中加入石灰石或生石灰作固硫剂,减少二氧化碳的排放 | |
| B. | 控制PM2.5的排放以减少雾霾天气 | |
| C. | 将盗版光盘碾压粉碎后回收再利用 | |
| D. | 提倡节日大量燃放烟花爆竹,增加喜庆气氛 |
1.下列实验操作,正确的是( )
| A. | 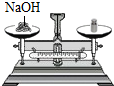 称量NaOH固体 | B. | 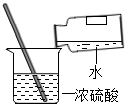 稀释浓硫酸 | C. | 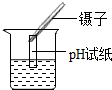 测定溶液的pH | D. |  闻药品的气味 |



