题目内容
8.发射通信卫星的火箭用联氨(N2H4)做燃料,用四氧化二氮(N2O4)助燃,生成物不会对大气造成污染.(1)反应的化学方程式为2N2H4+N2O4=3N2+4H2O,请在横线上填写化学式以完成该化学方程式.
(2)请计算3.2kg N3H4完全燃烧需要助燃物N2O4的质量.
分析 化学反应遵循质量守恒定律,即反应前后元素种类不变,原子种类和总个数都不变;
根据反应的化学方程式及其联氨的质量可以计算四氧化二氮的质量.
解答 解:(1)由反应可知,反应前后氢原子都是8个,氧原子都是4个,反应前氮原子是6个,反应后应该是6个,因此横线上的化学式应该是N2.
故填:N2.
(2)解:设需要助燃物N2O4的质量为x,
2N2H4+N2O4=3N2+4H2O,
64 92
3.2kg x
$\frac{64}{3.2kg}$=$\frac{92}{x}$,
x=4.6kg,
答:需要助燃物N2O4 的质量为4.6kg.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
18.济南素有“泉城”美誉,泉水富含硒、锶等十几种有益成分,其中硅酸盐具有软化血管、预防心血管病的作用.硅酸钠是泉水中主要的可溶性硅酸盐,已知在硅酸钠中硅元素的化合价为+4价,则硅酸钠化学式正确的是( )
| A. | NaSiO2 | B. | Na2SiO3 | C. | Na2SiO2 | D. | NaSiO3 |
16.如图表示初中化学常见实验操作,其中正确的是( )
| A. |  点燃酒精灯 | B. |  检查装置的气密性 | ||
| C. |  读出液体的体积 | D. | 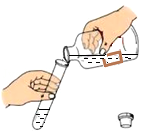 液体的取用 |
3.已知FeTiO3中钛的化合价为+4价,则铁的化合价为( )
| A. | +2 | B. | +3 | C. | 0 | D. | +1 |
13.下列符合“1+1=2”的事实是( )
| A. | 20℃,1L水与1L酒精混合后的体积等于2L | |
| B. | 20℃,1g锌与1g稀硫酸充分反应后所得的溶液质量为2g | |
| C. | 20℃,1g硫粉在1g氧气中完全燃烧后生成2g二氧化硫 | |
| D. | 20℃,1g镁与1g氧气反应得到2g氧化镁 |
20.空气是一种重要的资源.
(1)大气中二氧化碳含量过高会引起的环境问题是温室效应.
(2)人类时刻离不开空气,原因是空气中的氧气能供给呼吸.
(3)举出一个氮气在生产生活中应用的实例:食品防腐、保护气.
(1)大气中二氧化碳含量过高会引起的环境问题是温室效应.
(2)人类时刻离不开空气,原因是空气中的氧气能供给呼吸.
(3)举出一个氮气在生产生活中应用的实例:食品防腐、保护气.
17.以下是第三周期元素的原子半径及主要化合价(部分信息未列出).下列有关说法不正确的是( )
| 第三周期的部分元素 | Na | Mg | ① | Si | P | S | Cl |
| 原子的最外层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 原子半径(10-10m) | 1.86 | 1.60 | 1.43 | ② | 1.10 | 1.02 | 0.994 |
| 最高正价 最低负价 | +1 无 | +2 无 | +3 无 | +4 -4 | +5 -3 | +6 ③ | +7 -1 |
| A. | ②处的数值介于1.10-1.43之间 | |
| B. | 硫元素的最低负价为-2价 | |
| C. | 第三周期元素(Na-Cl)的最高正价数等于其原子的最外层电子数 | |
| D. | 硫化铝的化学式为AlS |
18.下列有关物质的组成或分类说法正确的是( )
| A. | 金属和金属合金都含有相同的元素 | B. | 熟石灰、生石灰都含有氢氧根离子 | ||
| C. | 生理盐水和石蕊溶液都是混合物 | D. | 钙和铁都是人体必需的微量元素 |