题目内容
根据下列两个实验分析完成下列问题:
(1)陈敏同学在实验室准备制取Cu(NO3)2,以铜和稀硝酸为主要原料设计了两种方案:
方案一:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑十4X;
方案二:2Cu+O2
2CuO,CuO+2HNO3=Cu(NO3)2+H2O.
从环境保护的角度考虑,你认为较合理的是方案 ,理由是 .
(2)李华同学在实验室要除去铜屑中的少量铁屑,设计了以下两个实验方案:

a.写出两个实验方案中有关反应的化学方程式:
① ,② .
b.以上两个实验方案中,你愿意选择的是 ,理由是 .
(1)陈敏同学在实验室准备制取Cu(NO3)2,以铜和稀硝酸为主要原料设计了两种方案:
方案一:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑十4X;
方案二:2Cu+O2
| ||
从环境保护的角度考虑,你认为较合理的是方案
(2)李华同学在实验室要除去铜屑中的少量铁屑,设计了以下两个实验方案:

a.写出两个实验方案中有关反应的化学方程式:
①
b.以上两个实验方案中,你愿意选择的是
考点:化学实验方案设计与评价,金属的化学性质,酸的化学性质,书写化学方程式、文字表达式、电离方程式
专题:简单实验方案的设计与评价
分析:(1)选择方案时要考虑是否产生有害气体污染空气,方案是否可行,是否安全,操作是否简单,是否节约了原料.
(2)根据铁和铜的化学性质可知,对于方案②铁能够与硫酸反应而铜不能与酸反应,且反应较易分离.而①中铁置换硫酸铜中的铜,虽然看起来增加了铜的质量,但是由于置换反应发生在铁的表面,导致铜在铁表面附着,从而阻碍反应的进行,导致铁铜难以分离和彻底反应且不能得到纯铜
(2)根据铁和铜的化学性质可知,对于方案②铁能够与硫酸反应而铜不能与酸反应,且反应较易分离.而①中铁置换硫酸铜中的铜,虽然看起来增加了铜的质量,但是由于置换反应发生在铁的表面,导致铜在铁表面附着,从而阻碍反应的进行,导致铁铜难以分离和彻底反应且不能得到纯铜
解答:解:(1)选择方案时要考虑是否产生有害气体污染空气,方案是否可行,是否安全,操作是否简单,是否节约了原料.方案一的生成物NO与氧气反应生成二氧化氮是有毒气体,会污染环境,故选方案二,并且制取相同质量的硝酸铜,方案二消耗的原料最少,硝酸中的硝酸根全部转化成了硝酸铜;
(2)铁和硫酸铜溶液反应生成铜和硫酸亚铁,反应的化学方程式:Fe+CuSO4═FeSO4+Cu;铁和硫酸反应生成氯化亚铁和氢气,反应的化学方程式:Fe+H2SO4═FeSO4+H2↑;方案②铁能够与硫酸反应而铜不能与酸反应,且反应较易分离.而①中铁置换硫酸铜中的铜,虽然看起来增加了铜的质量,但是由于置换反应发生在铁的表面,导致铜在铁表面附着,从而阻碍反应的进行,导致铁铜难以分离和彻底反应;
故答案为:
(1)二,
方案一的生成物NO与氧气反应生成二氧化氮是有毒气体,会污染环境,.
(2)a.①Fe+CuSO4═FeSO4+Cu,②Fe+H2SO4═FeSO4+H2↑.
b.②;方案②铁能够与硫酸反应而铜不能与硫酸反应,且反应较易分离.而①中铁置换硫酸铜中的铜,虽然看起来增加了铜的质量,但是由于置换反应发生在铁的表面,导致铜在铁表面附着,从而阻碍反应的进行,导致铁铜难以分离和彻底反应且不能得到纯铜;
(2)铁和硫酸铜溶液反应生成铜和硫酸亚铁,反应的化学方程式:Fe+CuSO4═FeSO4+Cu;铁和硫酸反应生成氯化亚铁和氢气,反应的化学方程式:Fe+H2SO4═FeSO4+H2↑;方案②铁能够与硫酸反应而铜不能与酸反应,且反应较易分离.而①中铁置换硫酸铜中的铜,虽然看起来增加了铜的质量,但是由于置换反应发生在铁的表面,导致铜在铁表面附着,从而阻碍反应的进行,导致铁铜难以分离和彻底反应;
故答案为:
(1)二,
方案一的生成物NO与氧气反应生成二氧化氮是有毒气体,会污染环境,.
(2)a.①Fe+CuSO4═FeSO4+Cu,②Fe+H2SO4═FeSO4+H2↑.
b.②;方案②铁能够与硫酸反应而铜不能与硫酸反应,且反应较易分离.而①中铁置换硫酸铜中的铜,虽然看起来增加了铜的质量,但是由于置换反应发生在铁的表面,导致铜在铁表面附着,从而阻碍反应的进行,导致铁铜难以分离和彻底反应且不能得到纯铜;
点评:本题考查学生根据所学的金属的性质来对除杂方案的评价能力,除杂问题是初中化学的一个难点;物理除杂和化学除杂,其中化学除杂选择试剂的原则是:不增、不减、不繁,最好的方法就是在除去杂质的同时又是原物质质量增加.

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
 利用陈化粮发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇的分子结构模型如图所示,下列关于乙醇的叙述正确的是( )
利用陈化粮发酵、蒸馏制得的乙醇被称为“绿色汽油”.乙醇的分子结构模型如图所示,下列关于乙醇的叙述正确的是( )| A、碳、氧元素的质量比为3﹕2 |
| B、相对分子质量为46 g |
| C、由碳、氢、氧三种原子构成的 |
| D、一个乙醇分子中含有3个氢分子 |
下列反应中,属于氧化反应,但不属于化合反应的是( )
A、碳+氧气
| ||
B、蜡烛+氧气
| ||
C、氢气+氧气
| ||
D、氧化汞
|
氧气是一种化学性质比较活泼的气体,它可以与许多物质发生化学反应,如图所示.关于三个反应叙述中不正确的是( )
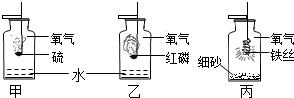

| A、都是化合反应 |
| B、反应都需要点燃;都放出热量 |
| C、甲中生成物是气体,乙、丙中生成物是固体 |
| D、甲中水和丙中细砂的作用完全一样 |
已知某两种物质在一定条件下发生化学反应,其微观示意图如图所示.下列说法正确的是( )


| A、该反应中共有四种分子 |
| B、该反应中反应物都是单质 |
| C、该反应不符合质量守恒定律 |
| D、该反应中生成物有单质和化合物 |
下列变化中不属于化学变化的是( )
| A、酒精燃烧 | B、榨取果汁 |
| C、面包发霉 | D、菜刀生锈 |
 所示,该元素原子的核电荷数为
所示,该元素原子的核电荷数为