题目内容
某化学课外活动小组为了测定石灰石中碳酸钙的含量,把10g石灰石固体样品进行高温煅烧,发生反应的化学方程式为:CaCO3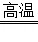 CaO+CO2↑.完全反应后,冷却、称量,残留固体质量7.8g.计算:(假设杂质不参加反应)
CaO+CO2↑.完全反应后,冷却、称量,残留固体质量7.8g.计算:(假设杂质不参加反应)
(1)固体质量减少了__________g,根据质量守恒定律,这是生成的___________(填具体物质名称或化学式)的质量.
(2)石灰石样品中碳酸钙的质量分数是多少?(要求写出计算过程)
 CaO+CO2↑.完全反应后,冷却、称量,残留固体质量7.8g.计算:(假设杂质不参加反应)
CaO+CO2↑.完全反应后,冷却、称量,残留固体质量7.8g.计算:(假设杂质不参加反应)(1)固体质量减少了__________g,根据质量守恒定律,这是生成的___________(填具体物质名称或化学式)的质量.
(2)石灰石样品中碳酸钙的质量分数是多少?(要求写出计算过程)
(1)2.2;二氧化碳(或CO2)
(2)设10g石灰石固体样品中含碳酸钙的质量为x,
CaCO3 CaO+CO2↑
CaO+CO2↑
100 44
x 2.2g
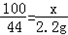 x=5g
x=5g
石灰石样品中碳酸钙的质量分数是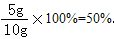
答:石灰石样品中碳酸钙的质量分数是50%.
(2)设10g石灰石固体样品中含碳酸钙的质量为x,
CaCO3
 CaO+CO2↑
CaO+CO2↑100 44
x 2.2g
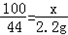 x=5g
x=5g石灰石样品中碳酸钙的质量分数是
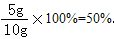
答:石灰石样品中碳酸钙的质量分数是50%.

练习册系列答案
相关题目
