题目内容
9.将下列物质敞口放置一段时间,物质变质且质量增加的是( )| A. | 浓硫酸 | B. | 浓盐酸 | C. | 熟石灰 | D. | 食盐 |
分析 变质即发生化学变化生成了新物质,然后根据常见物质的分析解答即可.
解答 解:A、浓硫酸具有吸水性而使质量增加,但不变质,故错误;
B、浓盐酸具有挥发性会使质量减少,所以错误;
C、熟石灰会吸收空气中的二氧化碳生成碳酸钙等,变质且质量增加.所以正确;
D、食盐在空气中不会质量增加和变质,所以错误;
故选C.
点评 本题综合考查常见酸碱盐的物理性质和化学性质,不仅要求考虑物质是否变质,还得分析物质质量的变化.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
4.用已知溶质质量分数的溶液可以测定未知溶液的溶质质量分数.实验室有一瓶标签模糊的稀盐酸,某同学为了测定其溶质质量分数,进行了如下实验:
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量;
②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量.数据如下表:
(1)若要配制500克16%的氢氧化钠溶液,需要氢氧化钠固体80克.
(2)本次实验中,实际消耗的氢氧化钠溶液质量为25克.
(3)请通过计算确定该瓶稀盐酸的溶质质量分数.
(4)另有同学做了同样的实验,却得到了不同的结果.于是用精密pH试纸测得反应后锥形瓶内溶液的pH为8.2,则他测出的盐酸溶质质量分数偏大(填“偏大”或“偏小”),造成这一偏差的原因是石蕊试液的变色不明显,你能改进这个测量过程吗?请简要描述改进方案;①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴酚酞试液(质量忽略不计),重新称量;②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由无色恰好变为红色时,停止滴加,再次称量.
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量;
②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量.数据如下表:
| 锥形瓶 | 锥形瓶+稀盐酸 | 锥形瓶+反应后溶液 | |
| 质量(克) | 35.5 | 55.5 | 80.5 |
(2)本次实验中,实际消耗的氢氧化钠溶液质量为25克.
(3)请通过计算确定该瓶稀盐酸的溶质质量分数.
(4)另有同学做了同样的实验,却得到了不同的结果.于是用精密pH试纸测得反应后锥形瓶内溶液的pH为8.2,则他测出的盐酸溶质质量分数偏大(填“偏大”或“偏小”),造成这一偏差的原因是石蕊试液的变色不明显,你能改进这个测量过程吗?请简要描述改进方案;①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴酚酞试液(质量忽略不计),重新称量;②往上述锥形瓶中逐滴加入溶质质量分数为16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由无色恰好变为红色时,停止滴加,再次称量.
4.如表是三种气体的密度(在0℃、101kPa条件下测定)和溶解程度.实验室要收集二氧化硫气体,可采取的方法是( )
| 气体 性质 | 氢气 | 二氧化碳 | 二氧化硫 |
| 密度(g•L-1) | 0.08987 | 1.975 | 2.716 |
| 溶解程度 | 极难溶于水 | 能溶于水 | 易溶于水 |
| A. | 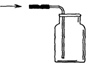 | B. | 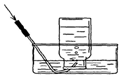 | C. |  | D. | 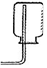 |
14.下列物质中能与盐酸反应,其生成物之一又能与石灰石反应的是( )
| A. | KOH | B. | AgNO3 | C. | CuSO4 | D. | Fe |
20.下列各物质分别久置于敞口的容器中,其质量增加且变质的是( )
| A. | 浓盐酸 | B. | 浓硫酸 | C. | 食盐 | D. | NaOH固体 |
 B.
B.  C.
C.  D.
D. 