题目内容
氯化钡是一种可溶性重金属盐,广泛应用于化工领域.用毒重石(主要成分为BaCO3)制备氯化钡晶体工艺流程如图: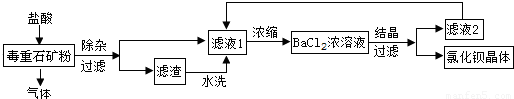
(1)毒重石要进行粉碎的目的是______.若所得滤液1仍浑浊,则应采取的操作是______.
(2)滤液2中可循环利用的物质除水外还有______.洗涤氯化钡晶体最适宜的洗涤剂是______(选填字母).
A.30℃水 B.30℃饱和氯化钠溶液 C.30℃饱和氯化钡溶液
(3)滤渣水洗的目的是______和______.
【答案】分析:(1)运用毒重石要进行粉碎能增大和盐酸的接触面积加快反应速率和过滤操作是为了除去液体中不溶性的固体杂质解答.
(2)运用碳酸钡和稀盐酸反应生成氯化钡和水还有二氧化碳,故滤液2是氯化钡的水溶液、洗涤氯化钡晶体不能再使其溶解解答.
(3)运用氯化钡属重金属盐对生产和生活不利,水洗滤渣即可提高生产率又可减少污染解答.
解答:解:(1)毒重石要进行粉碎能增大和盐酸的接触面积加快反应速率,滤液浑浊说明还有不溶性固体杂质再过滤,故答案:增大与反应物接触面积使反应更加充分 重新过滤
(2)碳酸钡和稀盐酸反应生成氯化钡和水还有二氧化碳 BaCl2,故滤液2是氯化钡的水溶液; 氯化钡溶于水,30℃饱和氯化钡溶液不能再溶解氯化钡,但30℃水和30℃饱和氯化钠溶液 都能溶解氯化钡,只能选择30℃饱和氯化钡溶液洗涤氯化钡晶体.故答案:BaCl2 C
(3)氯化钡属重金属盐对生产和生活不利,水洗滤渣即可提高生产率又可减少污染.故答案:提高原料的利用率(或提高产率) 减少可溶性重金属钡盐对环境的污染.
点评:本题是信息给予题,注意题中信息和课本知识的联系,看清每步操作的目的或反应实质即可较快解答.
(2)运用碳酸钡和稀盐酸反应生成氯化钡和水还有二氧化碳,故滤液2是氯化钡的水溶液、洗涤氯化钡晶体不能再使其溶解解答.
(3)运用氯化钡属重金属盐对生产和生活不利,水洗滤渣即可提高生产率又可减少污染解答.
解答:解:(1)毒重石要进行粉碎能增大和盐酸的接触面积加快反应速率,滤液浑浊说明还有不溶性固体杂质再过滤,故答案:增大与反应物接触面积使反应更加充分 重新过滤
(2)碳酸钡和稀盐酸反应生成氯化钡和水还有二氧化碳 BaCl2,故滤液2是氯化钡的水溶液; 氯化钡溶于水,30℃饱和氯化钡溶液不能再溶解氯化钡,但30℃水和30℃饱和氯化钠溶液 都能溶解氯化钡,只能选择30℃饱和氯化钡溶液洗涤氯化钡晶体.故答案:BaCl2 C
(3)氯化钡属重金属盐对生产和生活不利,水洗滤渣即可提高生产率又可减少污染.故答案:提高原料的利用率(或提高产率) 减少可溶性重金属钡盐对环境的污染.
点评:本题是信息给予题,注意题中信息和课本知识的联系,看清每步操作的目的或反应实质即可较快解答.

练习册系列答案
相关题目
亚硫酸钠(Na2SO3)在生活中可作防腐剂,在印染工业作为脱氧剂和漂白剂,现在实验存放较久的白色亚硫酸钠,学校的化学兴趣小组对它的成份进行探究.
查阅资料:
1亚硫酸钠在空气中易氧化成硫酸钠,不与二氧化碳反应
2亚硫酸钠溶液呈碱性,硫酸钠溶液呈中性
3亚硫酸钠与盐酸反应能生成盐、水和二氧化硫,与硝酸反应会氧化成硫酸钠
4亚硫酸钠与可溶性的钙、钡盐反应会产生白色沉淀
小芳阅读了上述的资料后,对这瓶白色固体进行了猜想与探究
猜想:
a白色粉末只有Na2SO3
b白色粉末只有______
c白色粉末是Na2SO3与Na2SO4的混合物
为了验证b的猜想,小芳选取了无色酚酞溶液、氯化钡溶液、稀硝酸中的一种进行以下探究,请帮她完成.
为进一步验证该白色粉末的组成,小麦做了以下的实验:
查阅资料:
1亚硫酸钠在空气中易氧化成硫酸钠,不与二氧化碳反应
2亚硫酸钠溶液呈碱性,硫酸钠溶液呈中性
3亚硫酸钠与盐酸反应能生成盐、水和二氧化硫,与硝酸反应会氧化成硫酸钠
4亚硫酸钠与可溶性的钙、钡盐反应会产生白色沉淀
小芳阅读了上述的资料后,对这瓶白色固体进行了猜想与探究
猜想:
a白色粉末只有Na2SO3
b白色粉末只有______
c白色粉末是Na2SO3与Na2SO4的混合物
为了验证b的猜想,小芳选取了无色酚酞溶液、氯化钡溶液、稀硝酸中的一种进行以下探究,请帮她完成.
| 实验操作 | 现象 | 结论 |
| 取样品置于烧杯中,加入 ______; | ______; | 猜想b不成立 |
| 实验操作 | 现象 | 结论 |
| 取14.6g的白色固体,加入 ______; | 有气体产生 | 证明白色固体肯定含有______; 可能含有______. |
| 把上述气体通入氢氧化钠溶液中,测得其增重6.4g | 确认白色固体是______. |
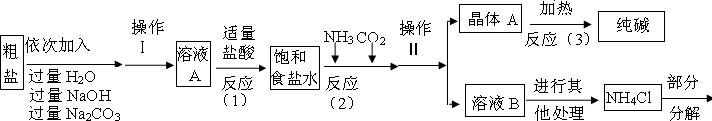
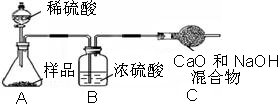 小心蒸发,并将所得物质干燥、冷却至室温后称得固体质量为13.1g.样品中碳酸钠的质量分数为
小心蒸发,并将所得物质干燥、冷却至室温后称得固体质量为13.1g.样品中碳酸钠的质量分数为
 小心蒸发,并将所得物质干燥、冷却至室温后称得固体质量为13.1g.样品中碳酸钠的质量分数为______(必须要有写出计算过程,请在下方写出)
小心蒸发,并将所得物质干燥、冷却至室温后称得固体质量为13.1g.样品中碳酸钠的质量分数为______(必须要有写出计算过程,请在下方写出)