题目内容
用“侯氏制碱法”制得的纯碱中常含有少量的氯化钠。为测定某纯碱样品中碳酸钠的质量分数,小明称取该样品11g,加入到盛有50g稀盐酸的烧杯中,恰好完全反应,称得烧杯中的溶液质量为56.6g。请计算:(1)完全反应后生成二氧化碳的质量为 g。
(2)该纯碱样品中碳酸钠的质量分数。(精确到0.1%)
(1)4.4g, (2) 96.4%
解析试题分析:(1) 根据题意可知,碳酸钠样品加入到盛有稀盐酸的烧杯中,二者反应生成氯化钠、水和二氧化碳,由于二氧化碳气体的逸出,烧杯中总物质的质量会减小,根据质量守恒定律可知,减少的质量为生成二氧化碳的质量=11g+50g-56.6g=4.4g。
(2) 根据题意,书写反应的化学方程式,可由二氧化碳的质量,利用方程式中二氧化碳与碳酸钠的质量比,计算出碳酸钠的质量,进而计算出样品中碳酸钠的质量分数。
解,设该纯碱样品中碳酸钠的质量为x
Na2CO3+2HCl="2NaCl+" CO2↑+H2O
106 44
x 4.4g
106:44=x:4.4g
解得,x=10.6g
则样品中碳酸钠的质量分数=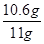 ×100% =96.4%
×100% =96.4%
答: 样品中碳酸钠的质量分数为96.4%。
考点:根据化学反应方程式的计算,质量守恒定律及其应用
点评:本题为根据化学方程式计算类问题中的简单计算,解题的关键是根据质量守恒定律找出生成二氧化碳的质量,然后依据已知量对未知的应求量进行求解计算即可;另外,注意解题要有完整的计算步骤和规范的书写格式。

练习册系列答案
 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案
相关题目