题目内容
16.某化学小组Ⅰ探究用大理石的盐酸反应制取二氧化碳气体,并进行性质实验.下图是有关实验的部分装置,请根据要求回答问题: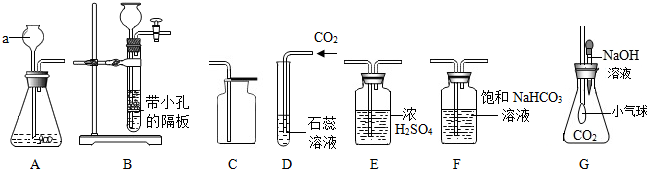
(1)a仪器的名称为长颈漏斗;
甲同学用A和C组合制取二氧化碳,乙同学用B和C组合制取二氧化碳,你认为哪个组合更便于控制反应乙(填写甲或乙).
(2)甲同学利用装置D进行性质实验时,观察到紫色石蕊试液变红色,将红色液体充分加热未能重新变为紫色,你认为可能的原因是通入的二氧化碳气体中含有少量氯化氢气体;为使上述红色液体加热后能重新变为紫色,在气体通往装置D之前可接入上图装置F(填写字母),在该装置中发生的主要化学反应方程式为NaHCO3+HCl=NaCl+H2O+CO2↑.
(3)乙同学将二氧化碳通入到氢氧化钠溶液中同,无明显现象,经过思考讨论后,设计了如图G装置,使该反应有了明显现象,则装置G中的现象为小气球逐渐膨胀起来或小气球变大.
分析 (1)熟记仪器的名称以及装置的特点来分析;
(2)根据盐酸具有挥发性进行分析;根据碳酸氢钠和盐酸反应会生成二氧化碳气体进行分析;
(3)根据二氧化碳会与氢氧化钠反应,导致锥形瓶内的压强减小进行分析.
解答 解:(1)a仪器的名称为长颈漏斗;B装置可以利用气体的压强将固体和液体分离,所以B装置更便于控制反应速率;故填:长颈漏斗;乙;
(2)盐酸具有挥发性,所以甲同学利用装置D进行性质实验时,观察到紫色石蕊试液变红色,将红色液体充分加热未能重新变为紫色,原因是:通入的二氧化碳气体中含有少量氯化氢气体,为使上述红色液体加热后能重新变为紫色,在气体通入装置D之前可接入如图装置F,碳酸氢钠和盐酸反应会生成二氧化碳气体、氯化钠和水,化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑;故填:通入的二氧化碳气体中含有少量氯化氢气体,F,NaHCO3+HCl=NaCl+H2O+CO2↑;
(3)二氧化碳会与氢氧化钠反应,导致锥形瓶内的压强减小,所以装置G中的现象为小气球逐渐膨胀变大起来.故填:小气球逐渐膨胀起来或小气球变大.
点评 本题考查了实验室制取气体的发生装置、收集方法的选择以及气体的性质检验,可依据气体发生装置、收集方法的依据及气体的性质逐一分析.

练习册系列答案
相关题目
6.下列叙述正确的是( )
| A. | 将生锈的菜刀浸泡在食盐水中,可除去其表面的铁锈 | |
| B. | 不锈钢就是永不生锈的钢铁 | |
| C. | 淬火后的缝衣钢针易弯曲 | |
| D. | 用食醋可除去热水壶内壁的水垢 |
4.下列推理正确的是( )
| A. | 酸雨呈酸性,呈酸性的雨水一定是酸雨 | |
| B. | 中和反应生成盐和水,生成盐和水的反应一定是中和反应 | |
| C. | 碱性溶液能使酚酞溶液变红,能使酚酞溶液变红的溶液一定呈碱性 | |
| D. | 盐是由金属离子和酸根离子组成的,NH4NO3中没有金属离子,不属于盐 |
1. 如图是甲、乙、丙三种物质的溶解度曲线,将甲、乙、丙三种物质t1℃时的饱和溶液升温至t2℃,所得溶液的溶质质量分数关系正确的是( )
如图是甲、乙、丙三种物质的溶解度曲线,将甲、乙、丙三种物质t1℃时的饱和溶液升温至t2℃,所得溶液的溶质质量分数关系正确的是( )
 如图是甲、乙、丙三种物质的溶解度曲线,将甲、乙、丙三种物质t1℃时的饱和溶液升温至t2℃,所得溶液的溶质质量分数关系正确的是( )
如图是甲、乙、丙三种物质的溶解度曲线,将甲、乙、丙三种物质t1℃时的饱和溶液升温至t2℃,所得溶液的溶质质量分数关系正确的是( )| A. | 甲>乙>丙 | B. | 甲=乙=丙 | C. | 甲=乙>丙 | D. | 乙>甲>丙 |
8.下列不属于金属材料的是( )
| A. | 铁矿石 | B. | 钢 | C. | 青铜 | D. | 银 |
5.请你用相关的化学知识解答下列问题:
(1)氢氧化钠是化学实验室中常用的试剂.氢氧化钠固体曝露在空气中易变质,这一变化的化学方程式可表示为2NaOH+CO2═Na2CO3+H2O,所以氢氧化钠固体必须密封保存,可用稀盐酸来检验氢氧化钠固体是否已变质;
(2)某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如下表所示.
请分析上表,并回答下列问题:
该花汁可以(填“可以”或“不可以”)作酸碱指示剂,将大量蒸馏水加入烧碱溶液,再滴入黄色花汁,溶液显示绿色;蚊子叮咬人时射入蚁酸(具有酸的性质),使皮肤红肿、痛痒.要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的肥皂水,若用PH试纸测定食醋的酸碱度,则PH试纸变成红色;
(3)某地的硫酸厂由于技术不过关,排放的废气形成酸雨,使得当地的土壤呈酸性,改良酸性土壤可以使用熟石灰,正常雨水PH=5.6,原因是(用化学方程式表示)CO2+H2O═H2CO3.
(1)氢氧化钠是化学实验室中常用的试剂.氢氧化钠固体曝露在空气中易变质,这一变化的化学方程式可表示为2NaOH+CO2═Na2CO3+H2O,所以氢氧化钠固体必须密封保存,可用稀盐酸来检验氢氧化钠固体是否已变质;
(2)某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如下表所示.
| 试剂 | 稀盐酸 | 食醋 | 蔗糖水 | 蒸馏水 | 肥皂水 | 烧碱 溶液 |
| 颜色 | 红 | 红 | 黄 | 黄 | 绿 | 绿 |
该花汁可以(填“可以”或“不可以”)作酸碱指示剂,将大量蒸馏水加入烧碱溶液,再滴入黄色花汁,溶液显示绿色;蚊子叮咬人时射入蚁酸(具有酸的性质),使皮肤红肿、痛痒.要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的肥皂水,若用PH试纸测定食醋的酸碱度,则PH试纸变成红色;
(3)某地的硫酸厂由于技术不过关,排放的废气形成酸雨,使得当地的土壤呈酸性,改良酸性土壤可以使用熟石灰,正常雨水PH=5.6,原因是(用化学方程式表示)CO2+H2O═H2CO3.
 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.