题目内容
5.向50g 20%的盐酸中,加入足量的镁,反应后所得溶液中溶质的质量分数为22.0%.分析 镁与稀盐酸反应生成氯化镁和氢气,由参加反应的稀盐酸的质量、溶质的质量分数,可以计算出参加反应的稀盐酸的质量,由反应的化学方程式列式计算出参加反应的镁的质量、生成氯化镁的质量、生成氢气的质量,进而计算出所得溶液中溶质的质量分数即可.
解答 解:50g 20%的盐酸中含溶质的质量为50g×20%=10g.
设生成氯化镁的质量为x,参加反应的镁的质量为y,生成氢气的质量为z,
Mg+2HCl═MgCl2+H2↑,
24 73 85 2
y 10g x z
$\frac{24}{y}=\frac{73}{10g}=\frac{85}{x}=\frac{2}{z}$
x=11.64g y=3.29g z=0.27g
所得溶液中溶质的质量分数为$\frac{11.64g}{3.29g+50g-0.27g}$×100%≈22.0%.
答:所得溶液中溶质的质量分数为22.0%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
15.下列实验操作叙述正确的是( )
| A. | 酒精着火用水扑灭 | |
| B. | 如无说明用量,固体物质取用1-2克 | |
| C. | 以节约为原则,用剩的药品要放回原瓶 | |
| D. | 玻璃仪器已洗干净的标准是内壁附着的水即不聚成水滴,也不成股流下 |
16.某小组对测定空气中氧气体积分数的实验进行了如下研究.
①完成测定空气中氧气体积分数的实验不适合选用下列哪种物质D;
A.汞B.磷C.铜D.木炭
②用甲、乙两套装置进行实验(红磷充足、装置不漏气).红磷燃烧的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,有关分析合理的是BC;
A.实验结束后装置内剩余气体只有氮气
B.甲中燃烧匙伸入集气瓶太慢,测得空气中氧气的体积分数将偏大
C.乙中的瘪气球可以防止燃烧放热使橡胶塞弹出
D.实验结束时未冷却到室温,测得空气中氧气的体积分数将偏大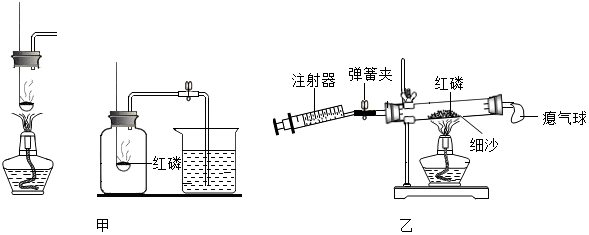
③利用乙装置实验时,先关闭弹簧夹,加热使红磷反应,待装置冷却至室温后打开弹簧夹.反应前后各数据及结论如下.
①完成测定空气中氧气体积分数的实验不适合选用下列哪种物质D;
A.汞B.磷C.铜D.木炭
②用甲、乙两套装置进行实验(红磷充足、装置不漏气).红磷燃烧的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,有关分析合理的是BC;
A.实验结束后装置内剩余气体只有氮气
B.甲中燃烧匙伸入集气瓶太慢,测得空气中氧气的体积分数将偏大
C.乙中的瘪气球可以防止燃烧放热使橡胶塞弹出
D.实验结束时未冷却到室温,测得空气中氧气的体积分数将偏大

③利用乙装置实验时,先关闭弹簧夹,加热使红磷反应,待装置冷却至室温后打开弹簧夹.反应前后各数据及结论如下.
| 玻璃管中原有空气的体积 | 注射器中气体的体积 | 结论 | |
| 反应前 | 反应后 | ||
| 50mL | 40 mL | 30 mL | 氧气约占空气体积的五分之一 |
10.下列为各种物质20℃时的溶解度,其中微溶物质是( )
| A. | 碳酸钙0.0013g | B. | 氢氧化钙0.17g | C. | 硼酸4g | D. | 硝酸钾31.6g |
2.下列对某一主题的知识归纳,正确的一组是( )
| A.节能减排 | B.物质与微观构成 |
| ?发展火力发电--解决电力紧张 ?汽油中乙醇--减少污染物排放 | ?桂花飘香--分子不停运动 ?热胀冷缩--分子大小改变 |
| C.化学与社会 | D.化学与能源 |
| ?合金、塑料--合成材料 ?患夜盲症--因为缺维生素C ?庄稼易倒伏、不抗旱--施氮肥 | ?沼气、酒精--生物能源,可再生能源 ?石 油、煤--化石能源,不可再生能源 |
| A. | A | B. | B | C. | C | D. | D |
20.日常生活中的下列做法,属于化学变化的是( )
| A. | 家庭自酿葡萄酒 | B. | 冰块给水产品保鲜 | ||
| C. | 直饮水机中活性炭吸附杂质 | D. | 铁水铸成铁锅 |
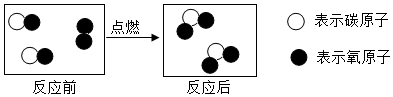
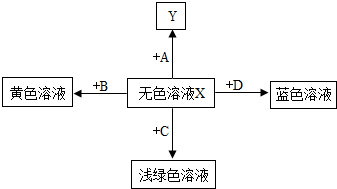 构建知识网络,可以帮助我们理解知识的内在联系.如图是某无色溶液X与不同类物质间反应的知识网络.请回答:
构建知识网络,可以帮助我们理解知识的内在联系.如图是某无色溶液X与不同类物质间反应的知识网络.请回答: