题目内容
在实验室用一氧化碳还原2.0 g赤铁矿样品,反应后生成的二氧化碳跟足量的澄清石灰水反应,生成了3.0 g白色沉淀。求赤铁矿样品中Fe2O3的质量分数。
.解:设生成3.0 g碳酸钙需要二氧化碳的质量为x
CO2+Ca(OH)2===CaCO3↓+H2O (1分)
44 100
x 3.0 g
![]() (2分)
(2分)
x=![]() =1.32 g (3分)
=1.32 g (3分)
设生成1.32 g二氧化碳需要Fe2O3的质量为y
Fe2O3+3CO![]() 2Fe+3CO2 (4分)
2Fe+3CO2 (4分)
160 132
y 1.32 g
![]() (5分)
(5分)
y=![]() =1.6 g (6分)
=1.6 g (6分)
赤铁矿样品中Fe2O3的质量分数为
![]() ×100% (7分)
×100% (7分)
=80% (8分)
答:赤铁矿样品中Fe2O3的质量分数为80%。

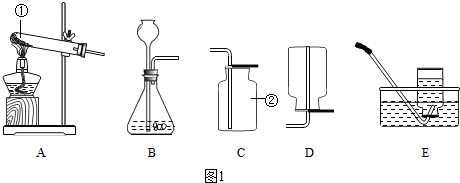
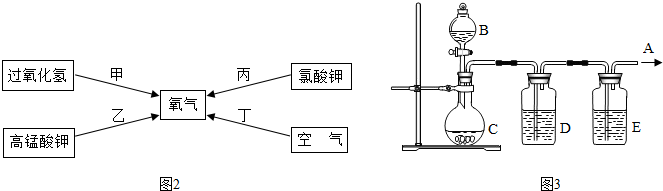
 李洋同学在实验室用木炭和氧化铜两种黑色粉末在高温下反应制取单质铜,反应的化学方程式为:C+2CuO
李洋同学在实验室用木炭和氧化铜两种黑色粉末在高温下反应制取单质铜,反应的化学方程式为:C+2CuO