题目内容
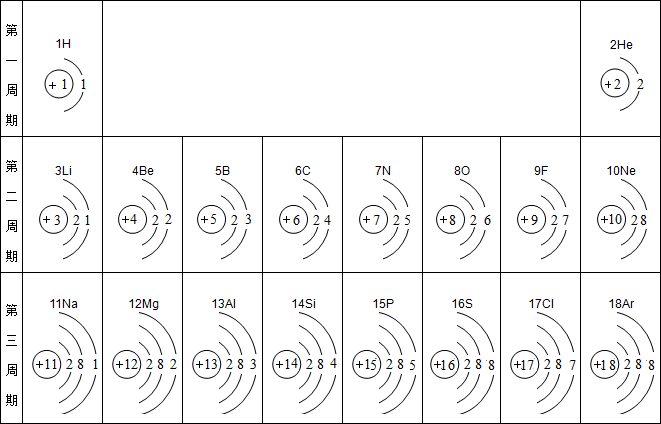
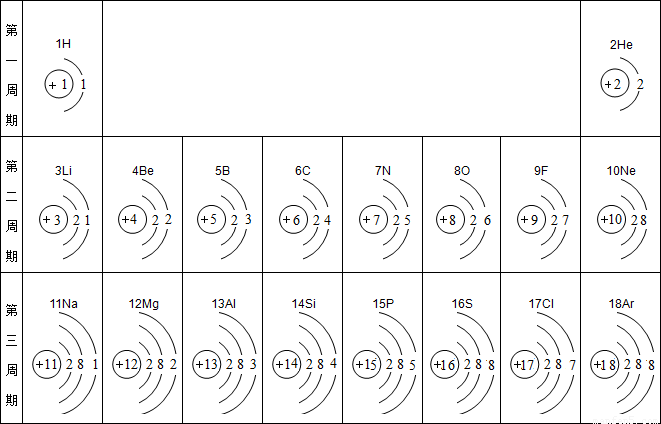
10、研究表明:在元素周期表中,最活泼的金属元素位于左下角,最活泼的非金属位于右上角(稀有气体除外).根据你所掌握的原子结构知识试回答以下问题:
(1)原子的电子层数和最外层电子数与该原子得失电子的能力有何关系?
(2)请你将你得出的结论与同学们交流,达成共识后再与老师一起探讨其原因.
(1)原子的电子层数和最外层电子数与该原子得失电子的能力有何关系?
(2)请你将你得出的结论与同学们交流,达成共识后再与老师一起探讨其原因.
分析:根据在元素周期表中,最活泼的金属元素位于左下角,最活泼的非金属位于右上角(稀有气体除外),可以得到电子层数越多,最外层电子数一定,越容易失去电子;电子层数越少,最外层电子数越多,越容易得到电子.则其原因可由原子结构来解释.
解答:解:(1)由最活泼的金属元素位于左下角,则原子的电子层数越多,在最外层电子数一定的条件下,就越容易失去电子;最活泼的非金属位于右上角(稀有气体除外),则在电子层数越少,最外层电子数越多,得到电子的能力就越强(稀有气体除外).
故答案为:电子层数相同时,最外层电子数越少,越容易失去电子,最外层电子数越多,越容易得到电子;最外层电子数相同时,电子层越多,越容易失去电子.
(2)分析原子的原子结构就会发现原子的结构存在规律性的变化,故答案为:原子的电子层数和最外层电子数与该原子得失电子的能力是原子结构的周期性变化的原因.
故答案为:电子层数相同时,最外层电子数越少,越容易失去电子,最外层电子数越多,越容易得到电子;最外层电子数相同时,电子层越多,越容易失去电子.
(2)分析原子的原子结构就会发现原子的结构存在规律性的变化,故答案为:原子的电子层数和最外层电子数与该原子得失电子的能力是原子结构的周期性变化的原因.
点评:本题具有一的难度,考查学生对问题的分析整合,归纳总结的能力,需要学生对元素周期表中前18号元素的原子结构熟练掌握.

练习册系列答案
相关题目
下表是元素周期表中1—18号元素的排列情况。根据此表我对它进行探究:
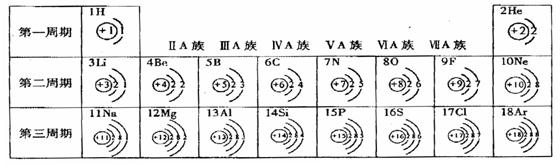 |
(1)通过对元素周期表的分析,我能得出的一条信息是 。
(2)第16号元素的名称是 ,第16号元素属于 元素(填“金属”或“非金属”),它的原子在化学反应中容易 电子(填“得”或“失”),它的离子符号为 。
(3)研究表明:在同一周期中,从左到右,原子失去电子的能力逐渐减弱,得到电子的能力逐渐增强。由此推断:第二周期中得电子能力最强的的是 原子;失电子能力最强的是 原子,具有稳定结构的是 原子。
(4)某元素的原子结构示意图为 ,则它位于元素周期表中的第 周期,该元素的化学性质与上表中第 族元素的化学性质相似。
,则它位于元素周期表中的第 周期,该元素的化学性质与上表中第 族元素的化学性质相似。


 ,则它位于元素周期表中的第
,则它位于元素周期表中的第