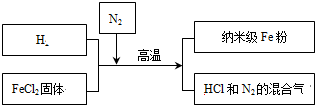
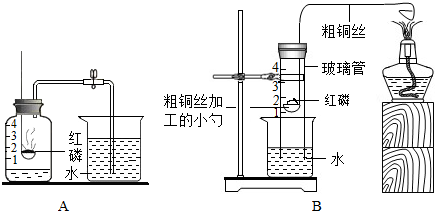
题目内容
碳酸钠和碳酸氢钠是生活中常见的盐,通过实验验证、探究它们的化学性质.
【查阅资料】
①Na2CO3+CaCO3=CaCO3↓+2NaCl ②2NaHCO3
Na2CO3+CO2↑+H2O ③Ca(HCO3)2 易溶于水.
④CaCl2溶液分别与 NaHCO3、Na2CO3溶液等体积混合现象(表中的百分数为溶液中溶质的质量分数):
【进行实验】
【解释与结论】
(1)实验1中,NaHCO3与盐酸反应的化学方程式为 .
(2)实验2中,试剂a为 .
(3)实验3中,NaHCO3与 CaCl+反应的化学方程式为:2NaHCO3+CaCl2═ + + +H2O.
【查阅资料】
①Na2CO3+CaCO3=CaCO3↓+2NaCl ②2NaHCO3
| ||
④CaCl2溶液分别与 NaHCO3、Na2CO3溶液等体积混合现象(表中的百分数为溶液中溶质的质量分数):
| NaHCO3 | Na2CO3 | ||||
| 0.1% | 1% | 5% | 0.1% | ||
CaCl2 | 0.1% | 无明显现象 | 有浑浊 | 有浑浊 | 有浑浊 |
| 1% | 无明显现象 | 有浑浊 | 有浑浊,有微小气泡 | 有沉淀 | |
| 5% | 无明显现象 | 有浑浊 | 有浑浊,有大量气泡 | 有沉淀 | |
| 序号 | 实验装置 | 主要实验步骤 | 实验现象 |
实验 1 |  | 向 2 支试管中分别加入少 量Na2CO3和NaHCO3溶液,再分别滴加盐酸 | 2 支试管中均有气泡产生 |
| 实验 2 |  | 向Ⅱ中加入试剂 a,向Ⅰ中 加入少量Na2CO3 或NaHCO3 固体,分别加热一 段时间 | Na 2CO3 受热时Ⅱ中无明显现象 NaHCO3受热时Ⅱ中出现 浑浊 |
实验 3 |  | 向Ⅱ中加入试剂 a,向Ⅰ中 加入少量 5%的 NaHCO3 溶 液,再滴加5%的 CaCl2 溶 液 | Ⅰ中出现浑浊,有气泡产 生Ⅱ中出现浑浊 |
(1)实验1中,NaHCO3与盐酸反应的化学方程式为
(2)实验2中,试剂a为
(3)实验3中,NaHCO3与 CaCl+反应的化学方程式为:2NaHCO3+CaCl2═
考点:实验探究物质的性质或变化规律,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)用质量守恒定律写碳酸氢钠和盐酸反应的化学方程式;
(2)从装置可看出是检验碳酸氢钠和碳酸钠的热稳定性,再结合二氧化碳能使澄清的石灰水变浑浊,分析解答.
(3)用质量守恒定律写NaHCO3 与 CaCl2 反应的化学方程式;
(2)从装置可看出是检验碳酸氢钠和碳酸钠的热稳定性,再结合二氧化碳能使澄清的石灰水变浑浊,分析解答.
(3)用质量守恒定律写NaHCO3 与 CaCl2 反应的化学方程式;
解答:解:
(1)碳酸氢钠和盐酸反应生成水和二氧化碳,故答案:NaHCO3+HCl═NaCl+H2O+CO2↑;
(2)本实验是为检验碳酸钠和碳酸氢钠的热稳定性.所以实验中的实验步骤是加热并将产生的气体通入澄清的石灰水中;
(3)NaHCO3与CaCl2反应的化学方程式2NaHCO3+CaCl2═CaCO3↓+2NaCl+CO2↑+H2O;
故答案为:
(1)NaHCO3+HCl═NaCl+H2O+CO2↑;
(2)澄清的石灰水;
(3)CaCO3↓,2NaCl,CO2↑;
(1)碳酸氢钠和盐酸反应生成水和二氧化碳,故答案:NaHCO3+HCl═NaCl+H2O+CO2↑;
(2)本实验是为检验碳酸钠和碳酸氢钠的热稳定性.所以实验中的实验步骤是加热并将产生的气体通入澄清的石灰水中;
(3)NaHCO3与CaCl2反应的化学方程式2NaHCO3+CaCl2═CaCO3↓+2NaCl+CO2↑+H2O;
故答案为:
(1)NaHCO3+HCl═NaCl+H2O+CO2↑;
(2)澄清的石灰水;
(3)CaCO3↓,2NaCl,CO2↑;
点评:典型的实验探究题,熟练掌握元素化合物的知识才能较快解答.碳酸盐和酸反应放出二氧化碳气体,二氧化碳能使石灰水变浑浊,碳酸盐溶液能和含钙离子的溶液反应生成沉淀.

练习册系列答案
相关题目
下列物质中属于混合物的是 ( )
| A、氮气 | B、二氧化碳 | C、水 | D、糖水 |
2013年3月,我国研制出世界上最轻、吸油能力最强的固体--碳海绵.碳海绵由碳元素组成,具有疏松多孔的结构.下列关于碳海绵的说法不正确的是( )
| A、碳海绵具有可燃性 |
| B、是一种新型的化合物 |
| C、具有较强的吸附性 |
| D、可处理海上泄露的石油 |