题目内容
15.水是生命之源、万物之基,是人类宝贵的自然资源,我们每个人都要爱护和节约.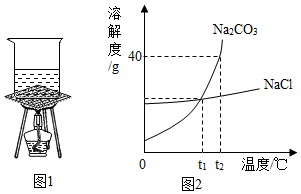
(1)自来水厂在净化水时,常加入活性炭以清除水中异色、异味、其净化原理是利用活性炭的吸附作用.
(2)小娟同学取一杯澄清的自来水,置于洁净的小烧杯中,用酒精灯加热,慢慢蒸发,水分蒸干后,观察到烧杯底部有少许白色固体残留,其原因是自来水中含有可溶性物质;
(3)我国有许多盐碱湖,湖中溶有大量氯化钠和纯碱,已知氯化钠和纯碱的溶解度曲线如图2所示:
①t2℃时碳酸钠的溶解度大于氯化钠的溶解度(填“大于”“小于”“等于”之一);
②将t2℃时氯化钠和碳酸钠的饱和溶液均降温到t1℃时,析出氯化钠晶体的质量无法确定析出碳酸钠晶体的质量(“大于”“小于”“等于”“无法确定”之一).
③t2℃时将40g碳酸钠固体加入50g水中,所得碳酸钠溶液中溶质与溶剂的质量比为2:5.
分析 活性炭有吸附作用,取一杯澄清的自来水,置于洁净的小烧杯中,用酒精灯加热,慢慢蒸发,水分蒸干后,观察到烧杯底部有少许白色固体残留,其原因是:自来水中含有可溶性物质;根据题目信息和溶解度曲线可知:碳酸钠、氯化钠两种固体物质的溶解度,都是随温度升高而增大,而碳酸钠的溶解度随温度的升高变化比氯化钠大;t2℃时碳酸钠的溶解度大于氯化钠的溶解度;将t2℃时氯化钠和碳酸钠的饱和溶液均降温到t1℃时,析出氯化钠晶体的质量与析出碳酸钠晶体的质量,无法确定大小;t2℃时将40g碳酸钠固体加入50g水中,所得碳酸钠溶液中溶质与溶剂的质量比=20g:50g=2:5.
解答 解:(1)活性炭有吸附作用,可以吸附一些染料、色素、异味等;故答案为:吸附;
(2)取一杯澄清的自来水,置于洁净的小烧杯中,用酒精灯加热,慢慢蒸发,水分蒸干后,观察到烧杯底部有少许白色固体残留,其原因是:自来水中含有可溶性物质;故答案为:自来水中含有可溶性物质;
(3)由溶解度曲线可知:t2℃时碳酸钠的溶解度大于氯化钠的溶解度;将t2℃时氯化钠和碳酸钠的饱和溶液均降温到t1℃时,析出氯化钠晶体的质量与析出碳酸钠晶体的质量,无法确定大小,因为没有说明饱和溶液的质量;t2℃时将40g碳酸钠固体加入50g水中,所得碳酸钠溶液中溶质与溶剂的质量比=20g:50g=2:5,故答案为:①大于;②无法确定;③2:5;
点评 本考点考查了活性炭的吸附作用、自来水的净化、溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
5.下列物质都属于纯净物的一组是( )
①冰水混合物 ②洁净的空气 ③液氮 ④石灰水.
①冰水混合物 ②洁净的空气 ③液氮 ④石灰水.
| A. | ②④ | B. | ①③ | C. | ①② | D. | ③④ |
6.甲、乙、丙、丁四种物质混合后,在一定的条件下充分反应,测得反应前后各物质的质量分数如下表所示.下列说法正确的是( )
| 甲 | 乙 | 丙 | 丁 | |
| 反应前质量分数/% | 70 | 15 | 6.25 | 8.75 |
| 反应后质量分数/% | 35 | 7.5 | 48.75 | 8.75 |
| A. | 甲和乙的质量之和一定等于生成的丙的质量 | |
| B. | 丁一定是该反应的催化剂 | |
| C. | 该反应的基本类型为分解反应 | |
| D. | 乙可能是单质,丙一定是化合物 |
10. 有一无色溶液X,分别加入氯化钡溶液、氢氧化钠溶液、氯化钠溶液,出现的现象如图所示,则溶液X是( )
有一无色溶液X,分别加入氯化钡溶液、氢氧化钠溶液、氯化钠溶液,出现的现象如图所示,则溶液X是( )
 有一无色溶液X,分别加入氯化钡溶液、氢氧化钠溶液、氯化钠溶液,出现的现象如图所示,则溶液X是( )
有一无色溶液X,分别加入氯化钡溶液、氢氧化钠溶液、氯化钠溶液,出现的现象如图所示,则溶液X是( )| A. | H2SO4溶液 | B. | (NH4)2SO4溶液 | C. | NH4Cl溶液 | D. | Na2CO3溶液 |
20.对下列事实的解释正确的是( )
| 事实 | 解释 | |
| A | 氧气用于切割金属 | 氧气有可燃性 |
| B | 洗洁精可用于除油污 | 洗洁精能溶解油污 |
| C | 打开汽水瓶盖有大量气泡冒出 | 温度升高,气体溶解度减小 |
| D | 可用排水集气法收集氧气 | 氧气难溶于水 |
| A. | A | B. | B | C. | C | D. | D |
7.由同种元素组成的不同单质叫做同素异形体,下列各组物质属于同素异形体的是( )
| A. | 冰和干冰 | B. | CO和CO2 | C. | 镁条和镁粉 | D. | 氧气与臭氧 |
4.下列物质的转化(“→”表示一种物质转化为另一种物质)中,每次转化只通过一步反应,不可能全部实现的是( )
| A. | H2O2→O2→CO2→H2CO3 | B. | NaOH→NaNO3→Na2CO3→NaCl | ||
| C. | CaCO3→CaO→Ca(OH)2→KOH | D. | Mg→H2→HCl→AlCl3 |