题目内容
小明同学将13.9 g含杂质的纯碱样品(碳酸钠与氯化钠的混合物)与90.5 g稀盐酸相混合,充分反应,测得反应生成气体的质量(m)与反应时间(t)的数据如下表所示:
| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 气体质量m/g | 0 | 0.88 | 1.76 | 2.64 | 3.52 | 4.4 | 4.4 |
根据题目要求,回答下列问题:
(1)碳酸钠完全反应后,生成CO2的质量为______ g。
(2)请在下面的坐标图中,画出反应生成气体的质量(m)随时间(t)变化的曲线。

(3)求完全反应后所得溶液中溶质的质量分数。(Na2CO3+2HCl===2NaCl+CO2↑+H2O)
答案:(1)4.4
(2)

(3)解:设样品中碳酸钠的质量为x,反应生成NaCl的质量为y。
Na2CO3+2HCl===2NaCl+CO2↑+H2O
106 117 44
x y 4.4 g
 =
= x=10.6 g
x=10.6 g
 =
= y=11.7 g
y=11.7 g
样品中氯化钠的质量为13.9 g-10.6 g=3.3 g
反应后溶液中溶质的质量=11.7 g+3.3 g=15 g
反应后溶液的质量=13.9 g+90.5 g-4.4 g=100 g
完全反应后所得溶液中溶质的质量分数为1 5%
5%
答:完全反应后所得溶液中溶质的质量分数为15%。

(9分)某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验。
I、实验方案
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,测得的pH逐渐变小直到pH小于7,则证明NaOH溶液与稀盐酸发生了化学反应。
⑴反应后,所得溶液显 性(填“酸”、“碱”或“中”)
⑵用pH试纸测定NaOH溶液pH时,正确的操作是:
。
⑶简述强调“测得的pH小于7”的理由:
______________________________________________________________________________。
方案二:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应。
该组同学将不同浓度的盐酸和NaOH溶液各10 克混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如下表)。
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65﹪ | 2.00﹪ | 3.5 |
| 2 | 3.65﹪ | 4.00﹪ | x |
| 3 | 7.30﹪ | 8.00﹪ | 14 |
⑸某同学在没使用温度计的情况下,通过下图所示装置完成了实验。则该同学根据实验现象:
,判断NaOH溶液与稀盐酸发生了中和反应。
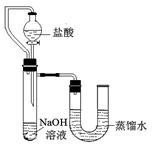
II、实验中的意外情况
在实验过程中,他们发现盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末。他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:①可能是NaOH;②可能是Na2CO3;③可能是NaOH和Na2CO3。
⑹小明同学取白色粉末少许,溶于水后,先向溶液中加入足量的 溶液,看到白色沉淀产生,然后向上层清液中加入酚酞试液,看到溶液呈红色,验证了猜想③是正确的。
⑺为了进一步研究,三位同学取了10.0g上述样品,利用电子天平共同做了下图所示的实验。

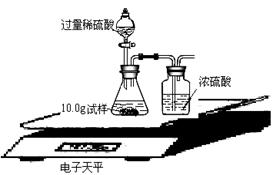
实验数据记录如下:
| 称 量 项 目 | 称 量 时间 | 质量(g) |
| 试样 | | 10.00 |
| 装置+稀硫酸质量 | | 241.20 |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 247.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 247.00 |
(8)有同学提出按上述实验所测得试样中Na2CO3质量分数会偏小,该同学的理由是(实验操作均正确): 。
金属材料和水在生产和生活中有着广泛应用。

(1)从右图是水的组成测定的实验,此反应的方程式为 。
(2)水是很好的溶剂。下表是KNO3和KCl在不同温度时的溶解度,请回答下列问题:
|
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
|
|
溶解度/g |
KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
|
KCl |
27.6 |
31.0 |
34.0 |
37.0 |
40.0 |
42.6 |
45.5 |
48.3 |
①40 ℃时,向两个分别盛有45 g KNO3和KCl固体的烧杯中,各加入100g的水,充分溶解后,结果如右图所示,则乙烧杯中的溶质是 。

②采用任意一种操作方法,将上述烧杯中的剩余固体全部溶解,并将溶液变为不饱和溶液。下列说法中正确的是 (填字母)。
A.溶剂质量可能不变 B.溶液中溶质的质量分数一定增大
C.溶液质量一定增大 D.可采用升温或加水的方法
(3)从下图可知金属具有导热性的是 。

A.铁锅 B.铜导线 C.铝箔
(4)铁制品在空气中会发生锈蚀,其原因是铁与空气中的 共同作用的结果。为防止钢铁制品的锈蚀,厨房中的铁锅和菜刀通常需做的防护是 (要求一种方法即可)。
(5)在探究金属的化学性质时,某同学将带锈铁钉放入稀盐酸中,观察到铁锈逐渐消失,溶液由无色逐渐变成黄色,并有气泡产生,有关反应的化学方程式为 、 。
(6)小明向含有FeSO4和CuSO4两种溶质的溶液中,加入一定质量镁粉,待充分反应后,滤液呈浅绿色。根据此现象作出了下列判断,你认为正确的是 (填写序号)。
A.滤纸上一定有Cu,可能有Fe,一定没有Mg
B.滤纸上一定有Fe,可能有Mg、Cu
C.滤液中一定有FeSO4,可能有MgSO4、CuSO4
D.滤液中一定有MgSO4、FeSO4,一定没有CuSO4
金属材料和水在生产和生活中有着广泛应用.
(1)如图1是水的组成测定的实验,此反应的方程式为 .
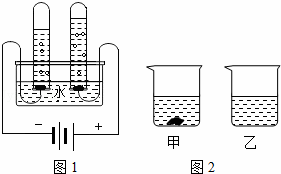
(2)水是很好的溶剂.下表是KNO3和KCl在不同温度时的溶解度,请回答下列问题:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
|
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 |
①40℃时,向两个分别盛有45g KNO3和KCl固体的烧杯中,各加入100g的水,充分溶解后,结果如图2所示,则乙烧杯中的溶质是 .
②采用任意一种操作方法,将上述烧杯中的剩余固体全部溶解,并将溶液变为不饱和溶液.下列说法中正确的是 (填字母).
A.溶剂质量可能不变 B.溶液中溶质的质量分数一定增大
C.溶液质量一定增大 D.可采用升温或加水的方法
(3)从下图可知金属具有导热性的是 .
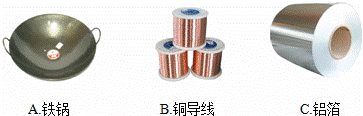
(4)铁制品在空气中会发生锈蚀,其原因是铁与空气中的 共同作用的结果.为防止钢铁制品的锈蚀,厨房中的铁锅和菜刀通常需做的防护是 (要求一种方法即可).
(5)在探究金属的化学性质时,某同学将带锈铁钉放入稀盐酸中,观察到铁锈逐渐消失,溶液由无色逐渐变成黄色,并有气泡产生,有关反应的化学方程式为 、 .
(6)小明向含有FeSO4和CuSO4两种溶质的溶液中,加入一定质量镁粉,待充分反应后,滤液呈浅绿色.根据此现象作出了下列判断,你认为正确的是 (填写序号).
A.滤纸上一定有Cu,可能有Fe,一定没有Mg
B.滤纸上一定有Fe,可能有Mg、Cu
C.滤液中一定有FeSO4,可能有MgSO4、CuSO4
D.滤液中一定有MgSO4、FeSO4,一定没有CuSO4.

