题目内容
13. 某钙片的标签如图所示,已知此钙片成分中只有碳酸钙含有钙元素.
某钙片的标签如图所示,已知此钙片成分中只有碳酸钙含有钙元素.(1)写出CaCO3中各元素的质量比10:3:12.
(2)请通过计算说明此标签中的含钙量是否错误.
分析 (1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)根据题意,每片含钙0.75g,每瓶50片,据此结合化合物的质量=该化合物中某元素的质量÷该元素的质量分数,进行分析解答.
解答 解:(1)碳酸钙中钙、碳、氧三种元素的质量比为40:12:(16×3)=10:3:12.
(2)每片含钙0.75g,每瓶50片,则每一瓶钙片的质量为0.75g÷($\frac{40}{40+12+16×3}×$100%)×50=93.75g.
93.75g>40g,故此标签中的含钙量错误.
故答案为:(1)10:3:12;(2)此标签中的含钙量错误.
点评 本题难度不大,考查同学们结合标签新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
3.“塑化剂”是一种重要的化工原料,属2B类致癌物,曾被添加到食品中,造成了“塑化剂”风暴.已知“塑化剂”的化学式为C24H34O4,下列说法正确的是( )
| A. | 该“塑化剂”属氧化物 | |
| B. | 该“塑化剂”中碳、氢、氧三种元素的质量比为12:17:2 | |
| C. | 该“塑化剂”中不含金属元素 | |
| D. | 该“塑化剂”,由24个碳原子、34个氢原子、4个氧原子构成 |
4.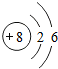 某元素的原子结构示意图如图,下列说法不正确的是( )
某元素的原子结构示意图如图,下列说法不正确的是( )
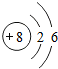 某元素的原子结构示意图如图,下列说法不正确的是( )
某元素的原子结构示意图如图,下列说法不正确的是( )| A. | 该元素属于非金属元素 | B. | 第一层上有2个电子 | ||
| C. | 该原子的质子数为8 | D. | 该原子容易失电子 |
1.小红是班里出了名的“粗心大王”,以下是从她的课堂笔记中摘录下来的部分物质的化学式,其中正确的是( )
| A. | 镁mg | B. | 氯化钠NaCL | C. | 氧化铜CuO | D. | 五氧化二磷2P5O |
18.关于相对原子质量,下列说法正确的是( )
| A. | 由于原子的质量数值太小,使用不方便,所以采用相对原子质量 | |
| B. | 相对原子质量是原子质量的简称 | |
| C. | 相对原子质量是以碳12原子的质量为标准的比值 | |
| D. | 碳的相对原子质量约是12g |
5.没有化学科学的发展,就没有今天丰富多彩的世界.下列过程与化学没有密切联系的是( )
| A. | 功能材料的制造 | B. | “天宫一号”航天轨道的设定 | ||
| C. | 医学上新型药物的研制 | D. | 新型清洁能源的开发和利用 |
3.化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
| A. | 为提高农作物的产量和质量,应大量使用化肥和农药 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 实现化石燃料清洁利用,就无需开发新能源 | |
| D. | 垃圾是放错地方的资源,应分类回收利用 |
 ,请据图回答下列问题.
,请据图回答下列问题.