题目内容
如图是某反应过程的微观示意图,“

”与“

分别表示不同元素的原子.图中X处的粒子示意图是( )


”与“

分别表示不同元素的原子.图中X处的粒子示意图是( )

A. | B. | C. | D. |
对比反应前后微粒的变化,去掉一个未反应的分子,得到各物质微粒的反应关系图为:
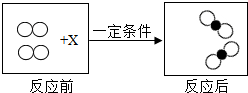
由质量守恒定律可知,反应前后原子的种类及数目不变,则图中X处的粒子示意图是
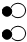
.由此可知,A、B、D错误,C正确.
故选C.

由质量守恒定律可知,反应前后原子的种类及数目不变,则图中X处的粒子示意图是
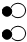
.由此可知,A、B、D错误,C正确.
故选C.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
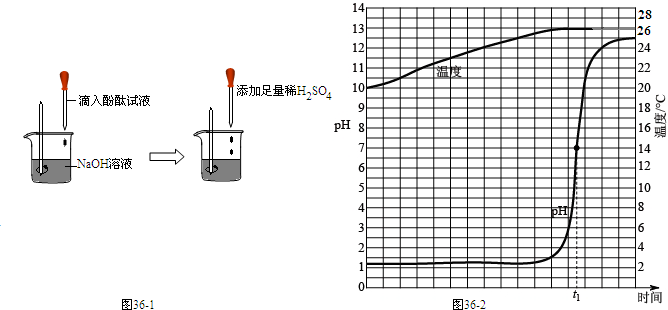
 下列是初三某合作学习小组实验室制取二氧化碳气体
下列是初三某合作学习小组实验室制取二氧化碳气体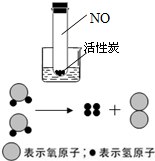 3月22日是“世界水日”,2011年“世界水日”的宣传主题为:“城市用水:应对都市化挑战”.水与人类的生活和生产密切相关.请回答以下相关问题:
3月22日是“世界水日”,2011年“世界水日”的宣传主题为:“城市用水:应对都市化挑战”.水与人类的生活和生产密切相关.请回答以下相关问题: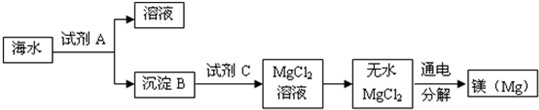
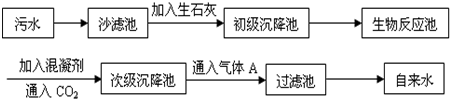
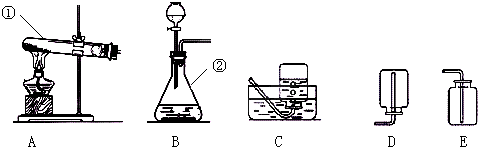
 3月22日是“世界水日”,2011年“世界水日”的宣传主题为:“城市用水:应对都市化挑战”.水与人类的生活和生产密切相关.请回答以下相关问题:
3月22日是“世界水日”,2011年“世界水日”的宣传主题为:“城市用水:应对都市化挑战”.水与人类的生活和生产密切相关.请回答以下相关问题:
