题目内容
鸡蛋壳的主要成分是碳酸钙.为了测定某鸡蛋壳中碳酸钙的质量分数,小群同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g 放在烧杯里,然后往烧杯中加入足量的稀盐酸90g,充分反应后,称得反应剩余物为97.8g.(假设其他物质不与盐酸反应,计算结果精确到0.1%)(1)产生二氧化碳气体______ g.
(2)计算该鸡蛋壳中碳酸钙的质量分数.
(3)反应后溶液中溶质的质量分数.
【答案】分析:(1)反应后剩余物的总质量比反应前的减少,根据质量守恒定律知,减少的质量就是生成二氧化碳的质量.
(2)由二氧化碳的质量根据碳酸钙与盐酸反应的化学方程式可以计算出鸡蛋壳中碳酸钙的质量分数.
(3)依据质量守恒定律可求反应后溶液的总质量,然后根据生成的氯化钙质量便可计算反应后溶液的溶质质量分数;
解答:解:(1)由质量守恒定律可知生成的二氧化碳质量是10g+90g-97.8g=2.2;
(2)设鸡蛋壳中CaCO3的质量为x,CaCl2的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 2.2g
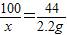 =
=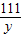
x=5g y=5.55g
鸡蛋壳中CaCO3的质量分数=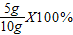 =50%
=50%
(3)CaCl2的质量分数=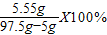 =6.0%
=6.0%
故答案为:(1)2.2;(2)蛋壳中CaCO3的质量分数为50%;(3)CaCl2的质量分数6.0%;
点评:答本题的关键是要知道固体质量的减少量就是生成二氧化碳的质量;根据气体的质量算出碳酸钙和氯化钙的质量,再计算质量分数即可.
(2)由二氧化碳的质量根据碳酸钙与盐酸反应的化学方程式可以计算出鸡蛋壳中碳酸钙的质量分数.
(3)依据质量守恒定律可求反应后溶液的总质量,然后根据生成的氯化钙质量便可计算反应后溶液的溶质质量分数;
解答:解:(1)由质量守恒定律可知生成的二氧化碳质量是10g+90g-97.8g=2.2;
(2)设鸡蛋壳中CaCO3的质量为x,CaCl2的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 2.2g
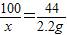 =
=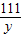
x=5g y=5.55g
鸡蛋壳中CaCO3的质量分数=
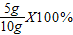 =50%
=50%(3)CaCl2的质量分数=
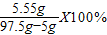 =6.0%
=6.0%故答案为:(1)2.2;(2)蛋壳中CaCO3的质量分数为50%;(3)CaCl2的质量分数6.0%;
点评:答本题的关键是要知道固体质量的减少量就是生成二氧化碳的质量;根据气体的质量算出碳酸钙和氯化钙的质量,再计算质量分数即可.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目