题目内容
如图所示,简要说明下列三种灭火器的灭火原理.

(1)泡沫灭火器(如图甲).筒内装入碳酸钠溶液,内瓶中装入盐酸溶液,其化学方程式是________,但这种泡沫灭火器喷出的药液具有腐蚀性.为此,当今泡沫灭器的药液已作了改进,筒内装入碳酸氢钠(NaHCO3)溶液,瓶内装入硫酸铝[Al2(SO4)3]溶液,其反应原理如下(要求配平下列化学方程式):
NaHCO3+Al2(SO4)3—Na2SO4+Al(OH)3↓+CO2↑其灭火原理是:________.
(2)液态CO2灭火器(如图乙).其灭火原理是________________.
(3)干粉灭火器(如图丙).其灭火原理是________________.
答案:
解析:
解析:
|
(1)Na2CO3+2HCl=2NaCl+CO2↑+H2O 6NaHCO3+Al2(SO4)3=3Na2SO4+2Al(OH)3↓ 6CO2↑ 以Na2SO4、Al(OH)3和CO2混合而形成的大量泡沫,其密度大于空气,并紧紧粘附在燃烧物上,隔绝空气加灭火 (2)液态CO2喷出后,吸热气化时温度急剧下降,使局部CO2凝聚成白色于冰(固体CO2),干冰颗粒或气态CO2在燃烧物周围形成严密封锁区,隔绝空气而灭火. (3)2NaHCO3 |

练习册系列答案
相关题目
 完成了本学期化学学习任务,化学兴趣小组的同学想利用所学的知识对“我们吸入的空气和呼出的气体有什么不同?”作进一步的探究,请你参与以下活动,完成空白部分的内容:
完成了本学期化学学习任务,化学兴趣小组的同学想利用所学的知识对“我们吸入的空气和呼出的气体有什么不同?”作进一步的探究,请你参与以下活动,完成空白部分的内容:
 已知氢气是最轻的气体单质,难溶于水.如图所示的装置(正立放置),既用作排水法收集氧气或氢气,又能用作排空气法收集氢气或二氧化碳,试分别简要加以说明,并指明气体流入和流出的方向.
已知氢气是最轻的气体单质,难溶于水.如图所示的装置(正立放置),既用作排水法收集氧气或氢气,又能用作排空气法收集氢气或二氧化碳,试分别简要加以说明,并指明气体流入和流出的方向.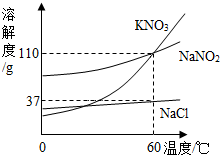 (2013?历下区二模)亚硝酸钠(NaNO2)常用作食品的发色剂和防腐剂,但食品中的亚硝酸钠含量超标会危害人体健康.亚硝酸钠具有咸味,外形和食盐很相似,亚硝酸钠的水溶液呈碱性.建筑行业常用亚硝酸钠作水泥添加剂,近年来,在建筑工地多次发生误将亚硝酸钠当作食盐食用导致中毒的事件.
(2013?历下区二模)亚硝酸钠(NaNO2)常用作食品的发色剂和防腐剂,但食品中的亚硝酸钠含量超标会危害人体健康.亚硝酸钠具有咸味,外形和食盐很相似,亚硝酸钠的水溶液呈碱性.建筑行业常用亚硝酸钠作水泥添加剂,近年来,在建筑工地多次发生误将亚硝酸钠当作食盐食用导致中毒的事件.