题目内容
20.用化学用语填空:(1)2个氢氧根离子2OH-;
(2)n个氮原子nN;
(3)标出五氧化二磷中磷元素的化合价$\stackrel{+5}{P}$2O5;
(4)2个氧气分子2O2;
(5)地壳中含量最多的元素与含量最多的金属元素组成的物质的化学式为Al2O3.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:(1)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字,故2个氢氧根离子可表示为:2OH-;
(2)原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.所以n个氮原子,就可表示为:nN;
(3)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以标出五氧化二磷中磷元素的化合价,故可表示为:$\stackrel{+5}{P}$2O5;
(4)分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,所以2个氧气分子可表示为2O2;
(5)地壳中含量最多的金属元素是铝元素,含量最多的非金属元素是氧元素,组成的化合物为氧化铝,氧化铝中铝元素显+3价,氧元素显-2价,其化学式为:Al2O3;
故答案为:(1)2OH-;(2)nN;(3)$\stackrel{+5}{P}$2O5;(4)2O2;(5)Al2O3;
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
相关题目
18.下列有关阿佛加德罗常数(NA)的说法错误的是( )
| A. | 22.4L O2所含的原子数目为NA | |
| B. | 0.5mol H2O含有的原子数目为1.5NA | |
| C. | 1mol H2O含有的H2O分子数目为NA | |
| D. | 0.5 NA个氯气分子的物质的量是0.5mol |
19.掌握科学的研究方法,探索化学世界的奥秘.
(1)分类是学习化学的重要方法之一,生活中常会接触到下列物质:A.铜丝B.天然气(主要成分为甲烷)C.冰水混合物D.二氧化硫E.氮气F.液态氧气G.高锰酸钾H.净化后的空气
其中属于混合物的是(填字母,下同)BH;属于氧化物的是CD,属于单质的是AEF.
(2)控制变量,设计对比实验是实验探究的重要方法.
(3)质量守恒定律是帮助我们学习和认识化学反应实质的重要理论.
①下列表述正确的是B.
A.蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B.每32gS和32gO2完全反应后,生成64gSO2
C.在化学反应aA+bB=cC+dD中一定有:a+b=c+d
②一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
则X的质量为34g;该反应所属的反应类型是分解反应;该反应中B和D两种物质变化的质量比为22:9.
(4)化学是在原子、分子的水平上研究物质及其变化规律,在宏观、微观和符号之间建立联系是化学学科的特点.
用“○”和“●”分别代表两种不同元素的原子,这两种元素组成的物质在一定条件下能发生一下反应,反应前后的微观模拟图如下:
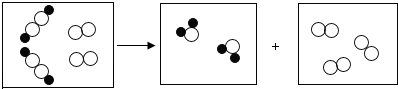
①该反应的基本反应类型是分解反应;
②据此可知化学反应前后原子的种类、个数不变;
③已知“○”的相对原子质量是“●”的m倍,该反应中生成物 与
与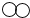 的质量比为(m+2):m.
的质量比为(m+2):m.
(1)分类是学习化学的重要方法之一,生活中常会接触到下列物质:A.铜丝B.天然气(主要成分为甲烷)C.冰水混合物D.二氧化硫E.氮气F.液态氧气G.高锰酸钾H.净化后的空气
其中属于混合物的是(填字母,下同)BH;属于氧化物的是CD,属于单质的是AEF.
(2)控制变量,设计对比实验是实验探究的重要方法.
| 实验编号 | ①探究人体呼出气体中二氧化碳含量比空气中的高 | ②探究影响品红扩散快慢的因素 | ③探究硫在空气和氧气中燃烧 |
| 实验设计 |  |  |  |
| 实验分析 | 本实验条件除了要控制两个盛装气体样品的集气瓶大小规格相同外,还要控制澄清石灰水体积相同. | 发现两杯水都变红,且整杯水变红时间比冷水要快,由此说明,分子在不断运动,影响分子运动快慢的因素有温度. | 取等量的硫粉点燃后,分别插入相同规格的盛有空气和氧气样品的集气瓶中,发现硫在氧气中燃烧更剧烈,该对比实验所得结论为O2含量越高,反应越剧烈. |
①下列表述正确的是B.
A.蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B.每32gS和32gO2完全反应后,生成64gSO2
C.在化学反应aA+bB=cC+dD中一定有:a+b=c+d
②一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
| 物质 | A | B | C | D |
| 反应前质量/g | 1.7 | 2.2 | 7.9 | 0.9 |
| 反应后质量/g | X | 6.6 | 0 | 2.7 |
(4)化学是在原子、分子的水平上研究物质及其变化规律,在宏观、微观和符号之间建立联系是化学学科的特点.
用“○”和“●”分别代表两种不同元素的原子,这两种元素组成的物质在一定条件下能发生一下反应,反应前后的微观模拟图如下:

①该反应的基本反应类型是分解反应;
②据此可知化学反应前后原子的种类、个数不变;
③已知“○”的相对原子质量是“●”的m倍,该反应中生成物
 与
与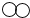 的质量比为(m+2):m.
的质量比为(m+2):m.
15.水是地球上最常见的物质之一,也是人类宝贵的自然资源.

(1)雪花被人们称为“冬之精灵”,世界上没有两片雪花的形状完全相同.下列说法正确的是D(填选项序号,下同).
A.雪花形成过程中,水分子由运动变为静止
B.雪花融化中,水分子间的间隔没有发生变化
C.不同雪花中,水分子的化学性质不相同
D.不同雪花中,水分子的数目都是巨大的
(2)在 TiO2 作催化剂和光照条件下,水能分解成氢气和氧气.该反应的化学方程式是2H2O$\frac{\underline{\;光照\;}}{TiO_{2}}$2H2↑+O2↑.
(3)电解水实验揭示了水的组成.图2实验中得到氧气的试管是2(填“1”或“2”).
(4)海水淡化可缓解淡水资源匮乏的问题.图3为太阳能海水淡化装置示意图.
①水变成水蒸气的过程中,不发生变化的是B(填字母序号)
A.分子质量B.分子种类C.分子间隔
②利用该装置将一定量的海水暴晒一段时间后,剩余海水中氯化钠的含量会不变(填“变大”“变小”或“不变”).
(5)图4是自来水厂净水过程示意图

【资料】我国生活饮用水的标准
请回答下列问题:
①下列关于水的叙述中,正确的是ACD.
A.过滤后的湖水不是纯净物B.水体有自净能力,不会被污染
C.工业废水经处理达标后才能排放D.明矾是常用的絮凝剂,可以用来净水
②根据上图信息,生产自来水时使用的净水方法有ABCE(填字母序号).
A.沉淀B.过滤C.投药消毒D.蒸馏E.吸附
利用活性炭去除异味和色素,活性炭的作用是吸附.家庭可采用如图5所示装置进行吸附操作,其中水样从下端入水口进入的主要目的是使水流速度降低利于活性炭的吸附.

(1)雪花被人们称为“冬之精灵”,世界上没有两片雪花的形状完全相同.下列说法正确的是D(填选项序号,下同).
A.雪花形成过程中,水分子由运动变为静止
B.雪花融化中,水分子间的间隔没有发生变化
C.不同雪花中,水分子的化学性质不相同
D.不同雪花中,水分子的数目都是巨大的
(2)在 TiO2 作催化剂和光照条件下,水能分解成氢气和氧气.该反应的化学方程式是2H2O$\frac{\underline{\;光照\;}}{TiO_{2}}$2H2↑+O2↑.
(3)电解水实验揭示了水的组成.图2实验中得到氧气的试管是2(填“1”或“2”).
(4)海水淡化可缓解淡水资源匮乏的问题.图3为太阳能海水淡化装置示意图.
①水变成水蒸气的过程中,不发生变化的是B(填字母序号)
A.分子质量B.分子种类C.分子间隔
②利用该装置将一定量的海水暴晒一段时间后,剩余海水中氯化钠的含量会不变(填“变大”“变小”或“不变”).
(5)图4是自来水厂净水过程示意图

【资料】我国生活饮用水的标准
| 感官指标 | 化学指标 | 细菌学指标 |
| 水质无色无味且澄清透明 | pH 65~8.5;总硬度<250mg/L. (以碳酸钙计);铜<l0mg/L,…等 | 细茵总数<100个/mL等 |
①下列关于水的叙述中,正确的是ACD.
A.过滤后的湖水不是纯净物B.水体有自净能力,不会被污染
C.工业废水经处理达标后才能排放D.明矾是常用的絮凝剂,可以用来净水
②根据上图信息,生产自来水时使用的净水方法有ABCE(填字母序号).
A.沉淀B.过滤C.投药消毒D.蒸馏E.吸附
利用活性炭去除异味和色素,活性炭的作用是吸附.家庭可采用如图5所示装置进行吸附操作,其中水样从下端入水口进入的主要目的是使水流速度降低利于活性炭的吸附.
9.元素的化学性质主要取决于原子的( )
| A. | 质子数 | B. | 相对原子质量 | C. | 中子数 | D. | 最外层电子数 |
 (1)我们知道有多种途径可以获得氧气.如:
(1)我们知道有多种途径可以获得氧气.如: 滴管是实验室中常用的一种仪器,下面就请和它一起完成题目吧.
滴管是实验室中常用的一种仪器,下面就请和它一起完成题目吧.