题目内容
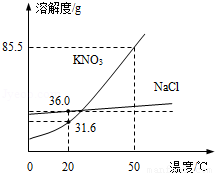
如图为NaCl、KNO3的溶解度曲线,回答下列问题:(1)20℃时,KNO3的溶解度是 g.
(2)某实验小组进行以下实验:10g水
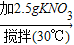 X
X 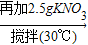 Y
Y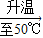 Z
ZX、Y、Z中为饱和溶液的是 .
(3)把NaCl的不饱和溶液变为饱和溶液,下列方法中一定可行的是 填序号)
A.降低温度 B.加入NaCl固体 C.蒸发溶剂.
【答案】分析:(1)据溶解度曲线可知某温度下物质的溶解度;
(2)根据硝酸钾的溶解度随温度变化情况及在20℃、50℃时的溶解度分析溶液的状态;
(3)不饱和溶液变为饱和溶液的一般方法是:增加溶质、蒸发溶剂、降温,氯化钠的溶解度随温度的升高变化不大.
解答:解:(1)20℃时,KNO3的溶解度是31.6g;
(2)KNO3的溶解度随温度的升高而逐渐增大,且KNO3在20℃、50℃时的溶解度分别是31.6g、85.5g,所以10g水在30℃时加入2.5gKNO3一定不不饱和,在50℃时10g水最多可溶解8.55gKNO3,所以Z也是不饱和溶液,则Y为饱和溶液;
(3)NaCl的溶解度受温度影响不大,所以把NaCl的不饱和溶液变为饱和溶液,可用蒸发溶剂的方法,不能用降温的方法,加入NaCl固体一定能使其不饱和溶液变为饱和溶液;
故答案为:(1)31.6;(2)Y;(3)BC.
点评:了解溶解度曲线的意义,并能结合相关知识分析解决相关问题,考查了学生对所学知识的掌握和应用能力.
(2)根据硝酸钾的溶解度随温度变化情况及在20℃、50℃时的溶解度分析溶液的状态;
(3)不饱和溶液变为饱和溶液的一般方法是:增加溶质、蒸发溶剂、降温,氯化钠的溶解度随温度的升高变化不大.
解答:解:(1)20℃时,KNO3的溶解度是31.6g;
(2)KNO3的溶解度随温度的升高而逐渐增大,且KNO3在20℃、50℃时的溶解度分别是31.6g、85.5g,所以10g水在30℃时加入2.5gKNO3一定不不饱和,在50℃时10g水最多可溶解8.55gKNO3,所以Z也是不饱和溶液,则Y为饱和溶液;
(3)NaCl的溶解度受温度影响不大,所以把NaCl的不饱和溶液变为饱和溶液,可用蒸发溶剂的方法,不能用降温的方法,加入NaCl固体一定能使其不饱和溶液变为饱和溶液;
故答案为:(1)31.6;(2)Y;(3)BC.
点评:了解溶解度曲线的意义,并能结合相关知识分析解决相关问题,考查了学生对所学知识的掌握和应用能力.

练习册系列答案
相关题目
 (2013?香洲区模拟)如图为NaCl、KNO3的溶解度曲线(水的密度约为1g/cm3).
(2013?香洲区模拟)如图为NaCl、KNO3的溶解度曲线(水的密度约为1g/cm3). (2013?白云区一模)下表是NaCl和KNO3在不同温度时的溶解度,请根据相关信息回答下列问题.
(2013?白云区一模)下表是NaCl和KNO3在不同温度时的溶解度,请根据相关信息回答下列问题. (2013?闵行区二模)如图为NaCl、KNO3的溶解度曲线(水的密度约为1g/cm3).
(2013?闵行区二模)如图为NaCl、KNO3的溶解度曲线(水的密度约为1g/cm3).
 (2012?连云港)如图为NaCl、KNO3的溶解度曲线(水的密度约为1g/cm3).
(2012?连云港)如图为NaCl、KNO3的溶解度曲线(水的密度约为1g/cm3). (2013?崇明县二模)如图为NaCl、KNO3的溶解度曲线
(2013?崇明县二模)如图为NaCl、KNO3的溶解度曲线