题目内容
14.海水中含有丰富的化学资源,利用海水中可值得食盐、纯碱等多种物质.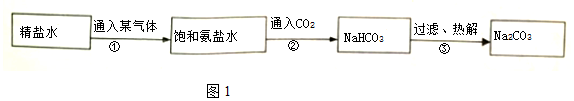
(1)我们的食用盐大部分来自于海水,从海水制取的粗盐中含有泥沙,硫酸镁和氯化钙等杂质,为得到较纯的氯化钠,可以将粗盐溶于水,然后进行如下操作:
①过滤②加过量的Na2CO3溶液③适量的盐酸④加过量的Ba(OH)2溶液⑤蒸发.正确的操作顺序是④②①③⑤(填序号).
(2)工业上采用氨碱法制纯碱的流程图如下:
在上述转化过程①中,通入的气体是NH3(填化学式),写出在上述转化过程中属于分解反应的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)Na2CO3和NaCl的溶解度曲线如图上述:试回答下列问题:
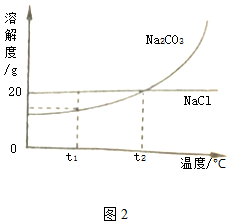
①若大量NaCl中混有少量Na2CO3的固体,可用蒸发结晶的方法提纯NaCl.
②t1℃时,将5g碳酸钠配制成饱和溶液,最多需要水的质量为25g.
分析 (1)除去硫酸镁用氢氧化钡,除去氯化钙用碳酸钠,碳酸钠还可以除去过量的氢氧化钡,所以先加氢氧化钡,再加碳酸钠,过滤除去沉淀和泥沙,再加入稀盐酸除去过量的碳酸钠,再蒸发可得到氯化钠;(2)精盐水变为铵盐水,缺少氮元素,所以气体是氨气;分解反应是碳酸氢钠加热得到碳酸钠、水和二氧化碳;(3)①氯化钠的溶解度随温度变化不大,所以用蒸发溶剂的方法;②根据t1℃时,碳酸钠的溶解度考虑.
解答 解:(1)除去硫酸镁用氢氧化钡,除去氯化钙用碳酸钠,碳酸钠还可以除去过量的氢氧化钡,所以先加氢氧化钡,再加碳酸钠,过滤除去沉淀和泥沙,再加入稀盐酸除去过量的碳酸钠,再蒸发可得到氯化钠,所以正确的操作顺序是④②①③⑤;
(2)精盐水变为铵盐水,缺少氮元素,所以气体是氨气;分解反应是碳酸氢钠加热得到碳酸钠、水和二氧化碳,所以方程式是:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
(3)①氯化钠的溶解度随温度变化不大,所以用蒸发溶剂的方法;②根据t2℃时,碳酸钠的溶解度是20g,所以100g水中最多溶解20g碳酸钠,所以25g水中最多溶解5g碳酸钠.
故答案为:(1)④②①③⑤(2)NH3; 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;(3)①蒸发结晶;②25.
点评 解答本题关键是熟悉溶解度曲线表示的意义,知道溶解度的四要素.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.实验室有一瓶久置的氢氧化钠固体,请你从所给的药品中选择合适的,设计实验证明出这瓶固体的成分.请在如表中填写实验操作步骤、判断依据、相应的结论.(注:器材选择不做要求,假设整瓶药品的变质程度是均匀的,实验方案要写全各种可能性.供选择的药品:蒸馏水、氯化钙溶液、稀盐酸、氢氧化钠溶液、酚酞溶液、石蕊试剂)
| 操作步骤 | 判断依据 | 对应结论 |
| 把适量固体置于试管中,加入足量水溶解,再加入足量氯化钙溶液,静置后滴加酚酞试液 | 不产生沉淀,溶液变红色,或产生白色沉淀,溶液变红色,或产生白色沉淀,溶液不变色 | 氢氧化钠没有变质,或氢氧化钠部分变质,或氢氧化钠全部变质 |
9.下列关于催化剂的说法正确的是( )
①催化剂在反应前后质量和化学性质没有改变、②催化剂就是MnO2、③催化剂加快了其他物质的化学反应速率、④催化剂改变了其他物质的化学反应速率.
①催化剂在反应前后质量和化学性质没有改变、②催化剂就是MnO2、③催化剂加快了其他物质的化学反应速率、④催化剂改变了其他物质的化学反应速率.
| A. | ①②③④ | B. | 只有①③④ | C. | 只有① | D. | 只有①④ |
19.我国化学家侯德榜改革了国外的纯碱生产工艺,发明了联合制碱法,其生产流程可简要表示如下: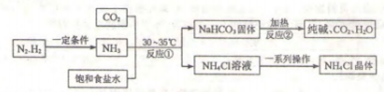
已知NH4Cl受热易分解,请回答下列问题.
(1)上述流程中可循环利用的物质是二氧化碳(写一种).
(2)反应②的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)下表是几种物质在不同温度下的溶解度.
分析表中数据可知,反应①中NaHCO3作为固体析出的原因是在室温时,碳酸氢钠的溶解度最小.上述流程中得到的NH4Cl溶液中一定有碳酸氢钠杂质,经一系列操作后,从NH4Cl溶液中获得NH4Cl晶体的方法是降温结晶.

已知NH4Cl受热易分解,请回答下列问题.
(1)上述流程中可循环利用的物质是二氧化碳(写一种).
(2)反应②的化学方程式是2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)下表是几种物质在不同温度下的溶解度.
| 温度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | - | - | - | - | |
| NaHCO3 | 6.9 | 8.2 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | - | |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.5 | 77.3 | |
3.甲、乙、丙三个集气瓶分别盛有空气、氧气、氮气中的一种,用一根燃着的木条分别插入瓶中,观察到的现象依次为:甲中火焰熄灭,乙中木条继续燃烧如初,丙中木条燃烧得更旺,则可判断出甲、乙、丙三瓶气体依次是( )
| A. | 氧气、氮气、空气 | B. | 氧气、空气、氮气 | C. | 空气、氮气、氧气 | D. | 氮气、空气、氧气 |
4.X、R表示两种元素,在溶液中发生反应:X+3RNO3=3R+X(NO3)3,下列说法不正确的是( )
| A. | 该反应是置换反应 | |
| B. | 若X是Al,R是Ag,则反应后溶液质量减少 | |
| C. | X的金属活动性比R强 | |
| D. | X可能是Fe,R可能是Cu |