题目内容
 过氧化氢溶液在存放过程中会缓慢分解.图示为实验室保存的一瓶过氧化氢溶液的标签.某小组同学为了解该瓶过氧化氢溶液是否分解,取50g该溶液共制得6.4g氧气.请通过计算得出该瓶过氧化氢溶液是否已部分分解.
过氧化氢溶液在存放过程中会缓慢分解.图示为实验室保存的一瓶过氧化氢溶液的标签.某小组同学为了解该瓶过氧化氢溶液是否分解,取50g该溶液共制得6.4g氧气.请通过计算得出该瓶过氧化氢溶液是否已部分分解.考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据标签所示计算出这瓶过氧化氢溶液原有过氧化氢的质量,然后根据过氧化氢缓慢分解的化学方程式,得出分解掉的过氧化氢的质量与生成水的关系式,再根据质量分数公式进行计算,即可得出分解掉的过氧化氢的质量.
解答:解:设生成6.4gO2需H2O2质量为x
2H2O2
2H2O+O2↑
68 32
x 6.4g
=
x=13.6g
所以此时该过氧化氢溶液的溶质的质量分数是
×100%=27.2%,而该瓶溶液标注的溶质质量分数为30%,故该瓶过氧化氢溶液在保存期间已部分分解.
2H2O2
| ||
68 32
x 6.4g
| 68 |
| x |
| 32 |
| 6.4g |
x=13.6g
所以此时该过氧化氢溶液的溶质的质量分数是
| 13.6g |
| 50g |
点评:本题主要考查学生运用化学方程式和质量分数公式进行计算的能力,难度不大,属基础性计算考查题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
青少年及成人缺乏某种微量元素将导致甲状腺肿大,且会造成智力损害,该微量元素是( )
| A、碘 | B、铁 | C、钙 | D、锌 |
根据日常经验和你所学的化学知识,判断下列变化没有发生化学变化的是( )
| A、瓷碗破碎 | B、铁锅生锈 |
| C、食物消化 | D、饭菜变馊 |
 (1)请指出图中存在的明显错误:
(1)请指出图中存在的明显错误: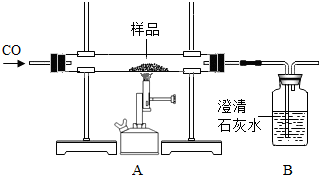

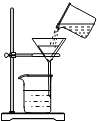 于博雅同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末,搅拌溶解,静置一会儿后,采用如图所示装置进行过滤.请问:
于博雅同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末,搅拌溶解,静置一会儿后,采用如图所示装置进行过滤.请问: