题目内容
已知:Cu2O+H2SO4== Cu+CuSO4+H2O。将14.4g Cu2O、Cu混合物溶于100.0g溶质质量分数为9.8%的稀H2SO4中,搅拌使之充分反应,过滤、洗涤、干燥得10.4g固体。下列说法正确的是
A. 10.4g固体是反应生成的铜的质量
B. 反应后溶液呈蓝色,溶质只有一种
C. 原混合物中Cu2O与Cu的质量之比为1∶1
D. 反应后溶液中CuSO4的溶质质量分数为8.0%
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案下列事实与相应的解释不一致的是( )
选项 | 事实 | 解释 |
A | 10mL酒精和10mL水混合后体积小于20mL | 混合后分子变小了 |
B | 氢氧化钠和氢氧化钙化学性质相似 | 在其溶液中都含有OH- |
C | 氮气常用作焊接金属时的保护气 | 氮气的化学性质不活泼 |
D | 一氧化碳与二氧化碳化学性质不同 | 分子的构成不同 |
A. A B. B C. C D. D
工业上生产电石(CaC2)并制备重要工业原料乙炔(CxHy)流程如图1所示:
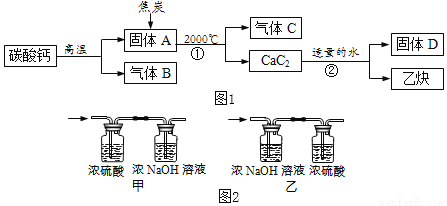
【资料】
①碳酸钙高温分解可得两种氧化物。
②浓硫酸具有强吸水性,NaOH溶液能吸收CO2。
【讨论】
(1)C、B组成元素相同,C有毒,反应①化学方程式为_____。
(2)D微溶于水,溶解度随温度升高而减小,D的化学式是_____。
【测定乙炔组成】
资料:一个乙炔分子有四个原子构成。
(3)将一定量的乙炔(CxHy)完全燃烧,并将生成的气体缓缓通过如图2所示的_____(选填“甲”或“乙”)装置,并再缓缓通一段时间的N2,并记录实验数据于如表中。
装置 | 反应前质量 | 反应后质量 |
浓硫酸 | 125.3g | 127.1g |
浓NaOH溶液 | 78.2g | 87.0g |
(4)实验中“缓缓通一段时间的N2”的目的是_____。
(5)计算:乙炔中碳元素质量为_____g,氢元素质量为_____g,乙炔化学式为_____。
(6)反应②的化学方程式为_____。



 Si+3M,M 可循环使用
Si+3M,M 可循环使用