题目内容
在“P+Q→盐和水”的反应中,物质P和Q不可能是( )
|
| A. | HCl,Ca(OH)2 | B. | SO2,NaOH | C. | Fe2O3,H2SO4 | D. | H2SO4,ZnCl2 |
考点:
物质的相互转化和制备;酸的化学性质;碱的化学性质.
专题:
物质的制备.
分析:
根据题意,“P+Q→盐和水”的反应中,生成物是盐和水,据此结合酸的化学性质(能与金属氧化物、碱等反应反应生成盐和水)、碱的化学性质(能与非金属氧化物反应生成盐和水),进行分析解答即可.
解答:
解:A、盐酸与氢氧化钙反应生成氯化钙和水,生成物是盐和水,故选项错误.
B、二氧化硫与氢氧化钠反应生成亚硫酸钠和水,生成物是盐和水,故选项错误.
C、氧化铁与硫酸反应生成硫酸铁和水,生成物是盐和水,故选项错误.
D、硫酸与氯化锌交换成分没有沉淀、气体或水生成,不能发生复分解反应,故物质P和Q不可能是硫酸与氯化锌,故选项正确.
故选:D.
点评:
本题难度不大,掌握酸的化学性质(能与金属氧化物、碱等反应反应生成盐和水)、碱的化学性质(能与非金属氧化物反应生成盐和水)并能灵活运用是正确解答本题的关键.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
我们每天扔掉的垃圾中,很多是宝贵的再生资源,因此生活中的垃圾要分类回收.下列物质中,属于可回收物的是( )
①纸张 ②塑料 ③玻璃 ④金属.
|
| A. | ①②③ | B. | ①③④ | C. | ②③④ | D. | ①②③④ |
小明设计了下列四组物质,要求在一定条件下都能一步转化,其中错误的是( )
|
| A. | Na2CO3→NaCl→NaNO3→NaOH | B. | C→CO→CO2→Na2CO3 |
|
| C. | Cu→CuO→CuSO4→Cu(OH)2 | D. | CaCO3→CaO→Ca(OH)2→NaOH |
 )。
)。

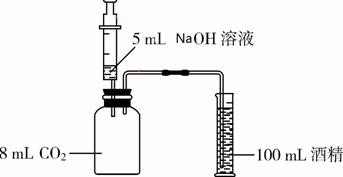
 . CO2不纯 b. 装置漏气
. CO2不纯 b. 装置漏气 CuSO4+SO2↑+2H2O,某小组同学用如图所示装置制取硫酸铜,请回答下列问题.
CuSO4+SO2↑+2H2O,某小组同学用如图所示装置制取硫酸铜,请回答下列问题.