题目内容
某化学兴趣小组的同学设计如下装置,测定不纯的氧化铜样品中铜元素的质量分数(杂质不参加反应且不含有铜元素).请同答下列问题: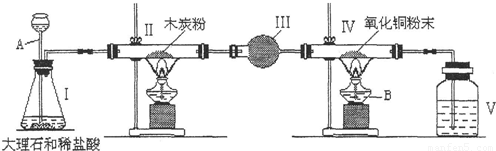
(1)指出标有字母的仪器的名称:A______ B______.
(2)写出Ⅰ装置中发生的化学反应方程式:______.
(3)指出Ⅲ装置的作用:______.
(4)写出硬质玻管Ⅱ中发生的化学方程式:______ 2CO
【答案】分析:(1)熟记常见仪器的名称;(2)根据方程式的写法考虑;(3)除去一氧化碳中的杂质;(4)根据反应物考虑发生的反应;(5)根据质量的减少量是氧化铜中氧元素的质量考虑;(6)缺少尾气处理装置.
解答:解:(1)要熟记常见仪器的名称和用途;
(2)反应物是碳酸钙和氯化氢,生成物是氯化钙、水、二氧化碳,用观察法配平即可,二氧化碳后面标上上升符号;
(3)用一氧化碳还原氧化铜时必须是纯净的一氧化碳,所以需要除去混在一氧化碳中的水蒸气和二氧化碳;
(4)反应物是碳和二氧化碳,生成物是一氧化碳,用观察法配平,反应条件是高温;
(5)根据方程式可知硬质玻管Ⅳ中的质量的减少量就是氧化铜中氧元素的质量,所以氧元素质量为:40.0g-38.4g=1.6g,根据氧化铜中铜元素与氧元素的质量比为64:16=4:1,所以铜元素质量为:1.6g×4=6.4g,又因为样品质量为:40g-30g=10g,所以样品中铜元素的质量分数为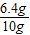 ×100%=64%;
×100%=64%;
(6)由于尾气中含有一氧化碳,有毒污染空气,所以要进行尾气处理装置.
故答案为:(1)A:长颈漏斗 B:酒精灯
(2)Ⅰ装置中的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)Ⅲ装置的作用:吸收水蒸气和未反应完的二氧化碳.
(4)玻管Ⅱ中的化学方程式:C+CO2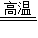 2CO.
2CO.
(5)铜元素的质量分数为64.0%.
(6)将装置V改为尖嘴导管,并用 燃着的酒精灯将导管排出的气体烧掉,或将装置V改为:
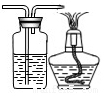
点评:通过回答本题知道了在组装反应装置时要注意尾气处理,不要污染空气,做到环保.
解答:解:(1)要熟记常见仪器的名称和用途;
(2)反应物是碳酸钙和氯化氢,生成物是氯化钙、水、二氧化碳,用观察法配平即可,二氧化碳后面标上上升符号;
(3)用一氧化碳还原氧化铜时必须是纯净的一氧化碳,所以需要除去混在一氧化碳中的水蒸气和二氧化碳;
(4)反应物是碳和二氧化碳,生成物是一氧化碳,用观察法配平,反应条件是高温;
(5)根据方程式可知硬质玻管Ⅳ中的质量的减少量就是氧化铜中氧元素的质量,所以氧元素质量为:40.0g-38.4g=1.6g,根据氧化铜中铜元素与氧元素的质量比为64:16=4:1,所以铜元素质量为:1.6g×4=6.4g,又因为样品质量为:40g-30g=10g,所以样品中铜元素的质量分数为
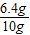 ×100%=64%;
×100%=64%;(6)由于尾气中含有一氧化碳,有毒污染空气,所以要进行尾气处理装置.
故答案为:(1)A:长颈漏斗 B:酒精灯
(2)Ⅰ装置中的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)Ⅲ装置的作用:吸收水蒸气和未反应完的二氧化碳.
(4)玻管Ⅱ中的化学方程式:C+CO2
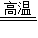 2CO.
2CO.(5)铜元素的质量分数为64.0%.
(6)将装置V改为尖嘴导管,并用 燃着的酒精灯将导管排出的气体烧掉,或将装置V改为:

点评:通过回答本题知道了在组装反应装置时要注意尾气处理,不要污染空气,做到环保.

练习册系列答案
相关题目
 12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.
12、碳酸氢钠(NaHCO3)俗称小苏打,常用于食品和医药工业.某化学兴趣小组的同学对碳酸氢钠的性质进行探究.


 (2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.
(2012?烟台)某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹. 某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.
某化学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.