题目内容
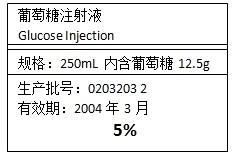 如图是病人输液时用的一瓶葡萄糖注射液标签,请你据图回答下列问题:
如图是病人输液时用的一瓶葡萄糖注射液标签,请你据图回答下列问题:(1)葡萄糖的化学式为C6H12O6,它由
(2)根据标签给出的数据,计算该溶液的密度为
考点:标签上标示的物质成分及其含量,相对分子质量的概念及其计算,元素质量比的计算
专题:标签图示型
分析:(1)①根据葡萄糖的化学式可知,它由哪几种元素组成;
②由葡萄糖的化学式可知,它的相对分子质量=(碳的相对原子质量×碳原子个数)+(氢的相对原子质量×氢原子个数)(氧的相对原子质量×氧原子个数);
③根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)溶液的密度=一瓶葡萄糖注射液的质量÷体积.
②由葡萄糖的化学式可知,它的相对分子质量=(碳的相对原子质量×碳原子个数)+(氢的相对原子质量×氢原子个数)(氧的相对原子质量×氧原子个数);
③根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(2)溶液的密度=一瓶葡萄糖注射液的质量÷体积.
解答:解:
(1)①由葡萄糖的化学式可知,它是由C、H、O这三种元素组成的;
②由葡萄糖的化学式可知,它的相对分子质量=12×6+1×12+16×6=180;
③C6H12O6中C、H、O元素的质量比为(12×6):(1×12):(16×6)=6:1:8.
(2)根据m=ρv和1ml=1cm3,则250cm3ρ=
,解得ρ=1g/cm3
故答案为:
(1)3;180;6:1:8;
(2)1.
(1)①由葡萄糖的化学式可知,它是由C、H、O这三种元素组成的;
②由葡萄糖的化学式可知,它的相对分子质量=12×6+1×12+16×6=180;
③C6H12O6中C、H、O元素的质量比为(12×6):(1×12):(16×6)=6:1:8.
(2)根据m=ρv和1ml=1cm3,则250cm3ρ=
| 12.5g |
| 5% |
故答案为:
(1)3;180;6:1:8;
(2)1.
点评:本题主要考查学生根据标签的有效信息,运用化学式进行计算的能力.

练习册系列答案
相关题目