题目内容
 如图是学生用来研究酸雨成因的实验用“催化棒”.这是由两根粗导线穿过橡皮塞固定在粗玻璃管中,B端用电热丝相连接而成.实验时,只要将A端导线连接直流电源使电热丝红热,然后将红热的电热丝伸入盛有SO2和空气的集气瓶中.
如图是学生用来研究酸雨成因的实验用“催化棒”.这是由两根粗导线穿过橡皮塞固定在粗玻璃管中,B端用电热丝相连接而成.实验时,只要将A端导线连接直流电源使电热丝红热,然后将红热的电热丝伸入盛有SO2和空气的集气瓶中.试回答:
(1)集气瓶中出现的现象:
(2)这个模拟实验得出酸雨的成因是:
(3)目前一座中等城市每年约燃煤300万吨,若煤的平均含硫量按1%计算,则每年将排放SO2
考点:酸雨的产生、危害及防治,盐的化学性质,化合物中某元素的质量计算
专题:化学与环境保护
分析:(1)根据二氧化硫和空气中的氧气还有水反应生成硫酸,硫酸和氯化钡反应生成硫酸钡白色沉淀分析;
(2)根据实验中实验步骤和设计分析;
(3)根据硫元素守恒去计算解答.
(2)根据实验中实验步骤和设计分析;
(3)根据硫元素守恒去计算解答.
解答:解:(1)二氧化硫和空气中的氧气还有水反应生成硫酸,硫酸和空气中的水蒸气结合成硫酸小液滴形成白雾;硫酸和氯化钡反应生成硫酸钡白色沉淀,故答案:出现白雾;生成白色沉淀.
(2)用电热棒加热二氧化硫和空气,所以酸雨的成因是空气中的SO2遇到矿尘或煤烟颗粒对SO2的固相催化作用就会形成酸雨,故答案:空气中的SO2遇到矿尘或煤烟颗粒对SO2的固相催化作用就会形成酸雨.
(3)煤中硫元素的质量是3000000t,煤中硫元素的质量为30000t,根据硫燃烧生成二氧化硫,二氧化硫和水反应生成硫酸,生成的二氧化硫有60%转化为H2SO4所以硫酸中的硫元素就是煤中硫的60%,故生成的硫酸中硫元素的质量为30000t×60%=18000t,硫酸中硫元素的质量分数为
,所以可得到98%的硫酸溶液的质量为
÷98%=56250t.
(2)用电热棒加热二氧化硫和空气,所以酸雨的成因是空气中的SO2遇到矿尘或煤烟颗粒对SO2的固相催化作用就会形成酸雨,故答案:空气中的SO2遇到矿尘或煤烟颗粒对SO2的固相催化作用就会形成酸雨.
(3)煤中硫元素的质量是3000000t,煤中硫元素的质量为30000t,根据硫燃烧生成二氧化硫,二氧化硫和水反应生成硫酸,生成的二氧化硫有60%转化为H2SO4所以硫酸中的硫元素就是煤中硫的60%,故生成的硫酸中硫元素的质量为30000t×60%=18000t,硫酸中硫元素的质量分数为
| 32 |
| 98 |
| 18000t | ||
|
点评:本题从实验和计算的角度考查了酸雨的形成,有一定的难度,计算时关键是利用好元素守恒的思想即可.

练习册系列答案
相关题目
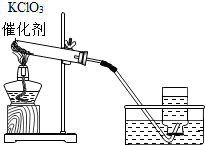 在实验室中用MnO2做为KClO3分解制氧气的催化剂:2KClO3
在实验室中用MnO2做为KClO3分解制氧气的催化剂:2KClO3 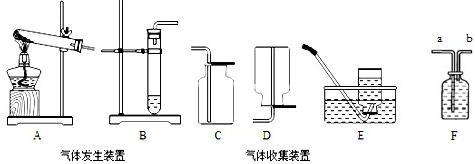
 如图所示:“空”的锥形瓶中充满了空气,小试管中盛有少量水,U形管中有适量水.现向小试管中加入适量生石灰.
如图所示:“空”的锥形瓶中充满了空气,小试管中盛有少量水,U形管中有适量水.现向小试管中加入适量生石灰.