题目内容
在工业上用纯碱和石灰石为原料制备烧碱,主要流程如图所示: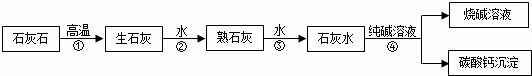
(1)在①﹣④四个过程中,发生了分解反应的是 (填序号).
(2)检验烧碱溶液中含有少量Na2CO3的具体方法是 .
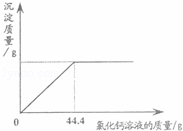
(3)在室温下,将53g质量分数为10%的Na2CO3溶液与3000g澄清石灰水充分混合,恰好完全反应.则这时所得NaOH溶液的质量是多少?(计算结果精确至0.1g)
①取适量溶液于试管中,滴加稀盐酸,若有气泡产生,则说明含有碳酸钠
解:设生成碳酸钙的质量为y,
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
106 100
53g×10% y
 =
=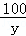 y=5g
y=5g
所以NaOH溶液的质量为:53g+3000g﹣5g=3048.0g.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
 物是中学化学学习和研究的重要内容。
物是中学化学学习和研究的重要内容。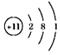 (1)右图是钠的原子结构示意图。下列说法不正确的是_______。
(1)右图是钠的原子结构示意图。下列说法不正确的是_______。 (2)钠与水反应生成氢氧化钠和氢气,化学方程式为________;小苏打受热分解成碳酸钠、二氧化碳和水,化学方程式为________。
(2)钠与水反应生成氢氧化钠和氢气,化学方程式为________;小苏打受热分解成碳酸钠、二氧化碳和水,化学方程式为________。 ,广泛用于航空、造船和化学工业中。工业上常用钠来制取钛,在高温时,钠与四氯化钛(TiCl4)反应生成氯化钠和钛。若用该方法制取2.4kg钛,理论上需要钠的质量是多少?
,广泛用于航空、造船和化学工业中。工业上常用钠来制取钛,在高温时,钠与四氯化钛(TiCl4)反应生成氯化钠和钛。若用该方法制取2.4kg钛,理论上需要钠的质量是多少?