题目内容
13.CO2和H2O是初中化学中出现频率较高的两种物质,不同种类的物质都可以通过化学反应生成它们,请按图中物质类别各选一种具体物质的化学式填在圆框旁,并按要求写出13个化学方程式: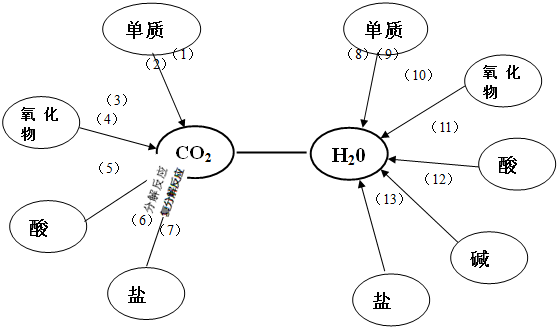
(1)C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,(2)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O,(3)2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2,(4)CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,(5)2HCl+Na2CO3=2NaCl+H2O+CO2↑,
(6)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,(7)CaCO3+2HCl=CaCl2+H2O+CO2↑,(8)2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,(9)H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,(10)CuO+2HCl=CuCl2+H2O,
(11)NaOH+HCl=NaCl+H2O,(12)2NaOH+CO2=Na2CO3+H2O,(13)CaCO3+2HCl=CaCl2+H2O+CO2↑.
分析 (1)根据碳和氧气在点燃的条件下生成二氧化碳进行分析;
(2)根据氧气和甲烷在点燃的条件下生成水和二氧化碳进行分析;
(3)根据一氧化碳和氧气在点燃的条件下生成二氧化碳进行分析;
(4)根据一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳进行分析;
(5)根据盐酸和碳酸钠反应生成氯化钠、水和二氧化碳进行分析;
(6)根据碳酸钙在高温的条件下生成氧化钙和二氧化碳进行分析;
(7)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(8)根据氢气和氧气在点燃的条件下生成水进行分析;
(9)根据氢气和氧化铜在加热的条件下生成铜和水进行分析;
(10)根据氧化铜和盐酸反应生成氯化铜和水进行分析;
(11)根据氢氧化钠和盐酸反应生成氯化钠和水进行分析;
(12)根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析;
(13)根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析.
解答 解:通过分析题中的反应关系和物质类别可知,
(1)碳和氧气在点燃的条件下生成二氧化碳,化学方程式为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;
(2)氧气和甲烷在点燃的条件下生成水和二氧化碳,化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(3)一氧化碳和氧气在点燃的条件下生成二氧化碳,化学方程式为:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
(4)一氧化碳和氧化铜在加热的条件下生成铜和二氧化碳,化学方程式为:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
(5)盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,化学方程式为:2HCl+Na2CO3=2NaCl+H2O+CO2↑;
(6)碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
(7)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(8)氢气和氧气在点燃的条件下生成水,化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(9)氢气和氧化铜在加热的条件下生成铜和水,化学方程式为:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
(10)氧化铜和盐酸反应生成氯化铜和水,化学方程式为:CuO+2HCl=CuCl2+H2O;
(11)氢氧化钠和盐酸反应生成氯化钠和水,化学方程式为:NaOH+HCl=NaCl+H2O;
(12)氢氧化钠和二氧化碳反应生成碳酸钠和水,化学方程式为:2NaOH+CO2=Na2CO3+H2O;
(13)碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
故答案为:
(1)C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;
(2)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(3)2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2;
(4)CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
(5)2HCl+Na2CO3=2NaCl+H2O+CO2↑;
(6)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
(7)CaCO3+2HCl=CaCl2+H2O+CO2↑;
(8)2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;
(9)H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
(10)CuO+2HCl=CuCl2+H2O;
(11)NaOH+HCl=NaCl+H2O;
(12)2NaOH+CO2=Na2CO3+H2O;
(13)CaCO3+2HCl=CaCl2+H2O+CO2↑.
点评 在解此类题时,首先分析应用的原理,然后找出反应物、生成物,最后结合方程式的书写规则书写方程式.

 阅读快车系列答案
阅读快车系列答案| 现 象 及 事 实 | 解 释 | |
| A | 100mL酒精和100mL水混合后,体积小于200mL | 分子大小没有发生改变 |
| B | 浓氨水敞口放置一段时间后,浓度变稀 | 分子是运动的 |
| C | 温度计的水银受热上升 | 分子是运动的 |
| D | 水通电后,电解生成氢气和氧气 | 分子是可以再分的 |
| A. | A | B. | B | C. | C | D. | D |