题目内容
小文收集到一瓶浑浊的长江水,他要模拟自来水厂的净水过程,最终制成蒸馏水.其实验过程如下所示.请回答以下问题.

(1)操作①的名称是 .
(2)操作②向滤液C中加入 ,利用其吸附性除去水样中的颜色和异味.
(3)小文取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多泡沫出现,说明液体D是 (填“硬水”、“软水”).
(4)自来水厂常用二氧化氯进行投药消毒,二氧化氯的化学式为 ,漂白粉(有效成分为次氯酸钙)也可作为饮水消毒剂,次氯酸钙[Ca(ClO)2]中氯元素的化合价为 .

(1)操作①的名称是
(2)操作②向滤液C中加入
(3)小文取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多泡沫出现,说明液体D是
(4)自来水厂常用二氧化氯进行投药消毒,二氧化氯的化学式为
考点:自来水的生产过程与净化方法,过滤的原理、方法及其应用,硬水与软水,化学式的书写及意义,有关元素化合价的计算
专题:空气与水
分析:(1)根据过滤的原理分析.
(2)根据水的净化过程及活性炭的吸附性分析.
(3)根据硬水、软水的鉴别方法分析.
(4)在化合物中,元素的化合价代数和为零,根据这一原则可以求出次氯酸钙中氯元素的化合价.
(2)根据水的净化过程及活性炭的吸附性分析.
(3)根据硬水、软水的鉴别方法分析.
(4)在化合物中,元素的化合价代数和为零,根据这一原则可以求出次氯酸钙中氯元素的化合价.
解答:解:(1)过滤是把不溶于液体的固体物质跟液体分离开来的一种混合物分离的方法;由净化河水的过程可知,需要将固液分开,所以,操作①的名称是过滤.
(2)由题意可知,过滤后的河水中常含有颜色和异味,可通过加入活性炭除去,此过程中没有新物质生成,主要发生物理变化.
(3)由于软水中不含或含有较少的可溶性的钙、镁化合物.所以,小刚取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多泡沫出现,说明液体D是软水.
(4)二氧化氯的化学式为:ClO2.故填:ClO2.
在次氯酸钙中,钙元素的化合价是+2价,氧元素的化合价是-2价,设氯元素的化合价为x
根据化合物中元素化合价代数和为零,(+2)+2x+(-2)×2=0,x=+1价.故填:+1.
答案:
(1)过滤.
(2)活性炭.
(3)软水.
(4)ClO2、+1.
(2)由题意可知,过滤后的河水中常含有颜色和异味,可通过加入活性炭除去,此过程中没有新物质生成,主要发生物理变化.
(3)由于软水中不含或含有较少的可溶性的钙、镁化合物.所以,小刚取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多泡沫出现,说明液体D是软水.
(4)二氧化氯的化学式为:ClO2.故填:ClO2.
在次氯酸钙中,钙元素的化合价是+2价,氧元素的化合价是-2价,设氯元素的化合价为x
根据化合物中元素化合价代数和为零,(+2)+2x+(-2)×2=0,x=+1价.故填:+1.
答案:
(1)过滤.
(2)活性炭.
(3)软水.
(4)ClO2、+1.
点评:本题以净化水为中心,同时考查了过滤操作、硬水和软水的区别和转化方法以及物理变化和化学变化的判断,解题时可结合所学知识,仔细分析解答.

练习册系列答案
相关题目
在一定温度下,某固态溶质(不含结晶水)的水溶液甲,经历如下变化:
溶液甲
溶液乙
溶液丙
下列结论正确的是( )
溶液甲
| 蒸发5g水 |
| 无晶体析出 |
| 蒸发5g水 |
| 析出2g晶体,过滤 |
下列结论正确的是( )
| A、溶液甲可能是饱和溶液 |
| B、溶液乙一定是不饱和溶液 |
| C、溶液乙和溶液丙中的溶质质量分数相等 |
| D、溶液丙若再蒸发5g水,析出的晶体可能大于2g |
在两个水分子(H2O)和两个硫化氢分子(H2S)中,含相同的( )
| A、氢原子 | B、氢元素 |
| C、氢气 | D、氢分子 |
正常雨水与酸雨的差异是( )
| A、正常雨水显中性,酸雨显酸性 |
| B、正常雨水的pH值约为5.6,酸雨的小于5.6 |
| C、正常雨水不含杂质,酸雨含杂质 |
| D、正常雨水降在农村,酸雨降在城市 |
将铁片投入下列溶液中,反应完毕后溶液的质量减少的是( )
| A、稀HCl |
| B、稀H2SO4 |
| C、CuSO4 |
| D、FeSO4 |

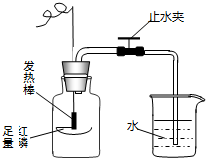 某兴趣小组同学按照如图实验装置进行实验,请回答相关问题:
某兴趣小组同学按照如图实验装置进行实验,请回答相关问题: