题目内容
8.实验室常用如图装置来制取氧气: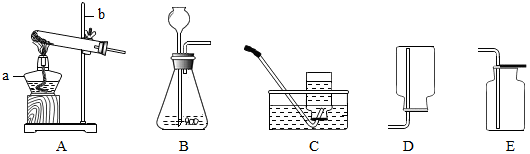
(1)写出图中有标号仪器的名称:a酒精灯、b铁架台.
(2)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是B(填序号),其中二氧化锰起催化作用.
(3)用氯酸钾制取氧气时,发生反应的文字表达式为氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气.
(4)用E装置收集氧气的依据是氧气的密度比空气大;当导管口开始有气泡产生时,不宜立即收集,原因是试管和导管中有空气;检验氧气是否集满的方法是把带火星的木条放在瓶口来验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了.
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小.氨气(NH3)极易溶于水.制取并收集氨气(NH3),应该从上图中选择的是A和D(填序号).
分析 (1)熟悉常见仪器,了解名称;
(2)根据双氧水是液体,二氧化锰是固体,也就是固液常温下的反应,选择发生装置;其中二氧化锰的作用是催化;
(3)根据已有的知识进行分析,加热氯酸钾能分解生成氯化钾和氧气;
(4)氧气的密度大于空气的密度,可以向上排空气法收集;根据氧气助燃性来验满;
用氯化铵固体与碱石灰固体共热来制取氨气的发生装置为“固体加热型”进行选择;常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,氨气极易溶于水,进行选择收集装置.
解答 解:(1)图中a是酒精灯,b是铁架台;
(2)用双氧水和二氧化锰来制取氧气,是固液常温下的反应,所以可以用B作为发生装置;其中的二氧化锰起到催化作用;
(3)根据已有的知识进行分析,加热氯酸钾能分解生成氯化钾和氧气,反应的文字表达式为:氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;
(4)E装置可以用来收集密度大于空气密度的气体,所以可以收集密度大于空气密度的氧气;因为试管和导管中有空气,因此当导管口开始有气泡产生时,不宜立即收集,否则氧气不纯;因为氧气有助燃的性质,所以验满是用带火星的木条放到集气瓶口,发现木条复燃,说明已满.故答案为:氧气密度比空气大、用带火星的木条放到集气瓶口,发现木条复燃,说明已满;
(5)用氯化铵固体与碱石灰固体共热来制取氨气的发生装置为“固体加热型”进行选择;常温下氨气是一种无色、有刺激性气味的气体,密度比空气小,氨气极易溶于水,进行选择收集装置.
故答案为:(1):酒精灯、铁架台;
(2)B、催化;
(3)氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;
(4)氧气的密度比空气大,试管和导管中有空气,把带火星的木条放在瓶口来验满,如果带火星的木条在瓶口能复燃,则证明该瓶氧气已经收集满了;
(5)A,D.
点评 本题主要考查实验装置的选取,以及气体的验满,要同学们了解常见气体的制取和性质.

 事物之间存在联系,找出联系、发现规律是我们学好化学的一种基本方法.
事物之间存在联系,找出联系、发现规律是我们学好化学的一种基本方法.(1)请你仿照下表中的示例,找出CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体之间存在的另外一个规律并排序.
| 规律 | 排序 |
| 示例:标准状况下,密度由大到小 | CO2、C2H4、C2H2、CH4 |
| 元素 | Na | Mg | ① | Si | P | ② | Cl |
| 原子的最外层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 原子半径(10-10m) | 1.86 | 1.60 | 1.43 | ③ | 1.10 | 1.02 | 0.994 |
| 最高正价 最低负价 | +1 | +2 | ④ | +4 -4 | +5 -3 | ⑤ | +7 -1 |
A.NO和O2+ B.CO和N2 C.NO2和CO2 D.SO2和C1O2
(4)A、B、C、D是初中化学常见的物质,且由H、C、O、S等4种元素中的一种或几种组成,它们之间的关系如图所示.(图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件均已略去).
已知A~D均含一种相同元素,A、B、D均为氧化物,A是目前计入空气污染指数的项目且它的一个分子中含有2个原子,B、D的元素组成相同且在常温下均为液态,B的相对分子质量比D的大,C是空气中的主要成分之一,请回答:
①A的化学式为CO;
②B→C反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
| A. | 1g酒精和1g水混合后的总质量 | |
| B. | 1g氧化铁和1g足量的稀盐酸反应后溶液的质量 | |
| C. | 1g饱和食盐水中加入1g食盐后,所得溶液的质量 | |
| D. | 1g氢氧化钠溶液和1g醋酸溶液混合后溶液的质量 |
| A. | 可能等于(a+b)g | B. | 可能小于(a+b)g | ||
| C. | 一定大于(a+b)g | D. | 可能小于或等于(a+b)g |
