题目内容
14. 碳及其化合物在生产、生活中应用广泛.
碳及其化合物在生产、生活中应用广泛.(1)干冰是由分子构成(填“分子”、“原子”或“离子”)
(2)天然气已替代煤炭成为家庭主要燃料,天然气相比煤炭的优点有天然气产生的二氧化碳少,放出的热量多(举1例)
(3)葡萄糖(C6H12O6)在酒化酶的催化下分解生成乙醇(C2H5OH)和一种含碳常见气体,该反应化学方程式为C6H12O6$\frac{\underline{\;酶\;}}{\;}$2C2H5OH+2CO2↑.
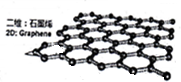
(4)石墨烯是从石墨材料中剥离出来,其剥离原理,就像我们将写错的字母胶条从纸上粘下来一样,石墨烯由碳原子组成的只有一层原子厚度的二维晶体(如图),图中每一个小球代表一个碳原子.它是目前发现的最薄、强度最大、导电导热性能最强的一种新型纳米材料.科学家甚至预言石墨烯将“彻底改变21世纪”.关于石墨烯,下列说法不正确的是B.
A.石墨烯由碳原子组成 B.石墨烯的化学性质稳定
C.石墨烯不溶于水 D.制作石墨烯过程属于化学变化.
分析 (1)根据干冰是由分子构成的解答;
(2)根据天然气产生的二氧化碳少,放出的热量多解答;
(3)根据葡萄糖转化为乙醇的同时能生成二氧化碳解答;
(4)根据题中信息进行分析解答.
解答 解:
(1)干冰是固体二氧化碳,二氧化碳是由分子构成的.
(2)然气已替代煤炭成为家庭主要燃料,天然气相比煤炭的优点有:天然气产生的二氧化碳少,放出的热量多;
(3)葡萄糖转化为乙醇的同时能生成二氧化碳,该反应化学方程式为:C6H12O6$\frac{\underline{\;酶\;}}{\;}$2C2H5OH+2CO2↑
(4)
A.石墨烯由碳原子构成,故说法正确;
B、常温下,石墨烯的化学性质稳定,故说法错误;
C、石墨烯不溶于水,故说法正确;
D、石墨与石墨烯是不同种物质,因此从石墨中剥离出石墨烯属于化学变化,故说法正确;
答案:
(1)分子;
(2)天然气产生的二氧化碳少,放出的热量多;
(3)C6H12O6$\frac{\underline{\;酶\;}}{\;}$2C2H5OH+2CO2↑
(4)B.
点评 环境污染日趋严重,已经引起人们的高度重视,治理污染初见成效,减少化石燃料的使用,大力开发利用新能源,有利于减缓环境污染.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.通过下列实验,可以得出的相应结论正确的是( )
| A. | 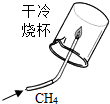 既说明甲烷具有可燃性,又说明甲烷是由氢元素和碳元素组成 | |
| B. |  既说明二氧化碳的密度比空气大,又说明二氧化碳不能燃烧也不支持燃烧 | |
| C. | 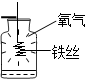 既说明铁丝具有可燃性,又说明增大氧气的浓度能促进燃烧 | |
| D. |  既说明二氧化碳可溶于水,又说明二氧化碳能与水反应 |
10.下列说法中,完全正确的是( )
| A. | 熄灭酒精灯可用嘴吹灭,加速溶解可用温度计搅拌 | |
| B. | 金属都能与酸溶液反应,合金的熔点都高于它的成分金属 | |
| C. | 硝酸钾属于复合肥,点燃羊毛会闻到烧焦羽毛的气味 | |
| D. | 肥皂水能将硬水转化为软水,高温下一氧化碳能将赤铁矿冶炼成纯铁 |
3.在某研究性学习小组调查发现,甲、乙两工厂排放的污水中含下列离子:H+、Cu2+、K+、NO3-、OH-中的三种离子(两厂含有一种相同的离子).若将两厂的污水按一定比例混合,沉淀后污水会变成无色澄清中性溶液.下列关于污水成分的分析,正确的是( )
| A. | H+和Cu2+来自同一工厂 | B. | Cu2+和K+来自同一工厂 | ||
| C. | H+和OH-来自同一工厂 | D. | OH-和Cu2-来自同一工厂 |