题目内容
某探究小组为测定赤铁矿中Fe2O3的质量分数,设计了如下装置,请回答:

(1)指出R仪器的名称是________.
(2)实验开始有如下操作:X:点燃酒精灯①,Y:点燃酒精灯②,Z:打开分液漏斗活塞,其操作顺序是________(用X、Y、Z填空).
(3)若缺少D装置,则会产生的后果是________,若实验只提供了一个酒精灯,则你的处理方法是________.
(4)我们还可用A装置在实验室制取的一种气体是________,其反应的化学方程式为________,该气体可用________法收集.
(5)该小组称耿此矿石样品10g,充分反应后得到的固体有7.6g,则样品中Fe2O3的质量分数为________.
(1)很显然R仪器的名称是铁架台;
(2)CO还原氧化铁反应前先通一段时间一氧化碳再加热,以免加热时CO与空气混合,可能引起爆炸,故答案为YZX;
(3)由于一氧化碳有毒,在关于该气体的实验都需要注意尾气的处理,点燃或收集.
(4)由装置图可知,A装置适合用于哪些不需加热,常温下就可进行的反应,因此A装置还可用于利用过氧化氢和二氧化锰的混合物制取氧气,故(4)问的答案为O2,2H2O2,
 2H2O+O2↑
2H2O+O2↑(5)根据质量守恒定律,氧化铁中氧元素的质量为10g-7.6g=2.4g,则样品中含氧化铁的质量为:2.4g÷30%=8g,则样品中Fe2O3的质量分数为8g÷10g×100%=80%,故答案是80%.
分析:本题以CO还原赤铁矿中的三氧化二铁为载体,重点考查了学生对实验仪器的装配或连接以及各组装置的作用的灵活运用能力;实际实验操作中遇到突发问题的处置能力和计算能力.
点评:本题是一道综合性的实验探究题,考查了的知识点较多.回答本题应注意化学用语的准确性及实验操作的完整性.

某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究。

【设计实验】用一氧化碳还原纯净的氧化铁粉末,实验装置如下图。
【进行实验】该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
【分析与讨论】本实验中,玻璃管内固体粉末由红色全部变为黑色。小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料。
【查阅资料】①CO还原Fe2O3的固体产物的成分与反应温度、反应时间等因素有关;
②CO还原Fe2O3的实验过程中固体产物可能有Fe3O4、FeO、Fe;
③NaOH溶液与石灰水相似,能吸收CO2,但不变浑。
④
|
物质性质 |
四氧化三铁 |
氧化亚铁 |
氧化铁 |
铁粉 |
|
颜色 |
黑色 |
黑色 |
红色 |
黑色 |
|
能否被磁铁吸引 |
能 |
不能 |
不能 |
能 |
【实验与猜想】
(1)该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和 。
(2)进行猜想:黑色固体粉末可能a.全部为铁、 b. 、c. 。
【得出结论】
(3)通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称) 。
【反思与评价】
(4)一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度。
(5)实验装置图中采用虚线框内的装置,其作用有 。

A.收集CO B.吸收CO2 C.检验CO2
【实践应用】小明和他的同学想测定某赤铁矿石中Fe2O3的质量分数。用CO与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用足量的NaOH溶液完全吸收,该溶液总质量与反应时间的变化关系如右图。
(6)上述反应产生CO2的质量为 g;
(7)计算该赤铁矿石中氧化铁的质量分数。 。(需要有计算过程)
某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究。
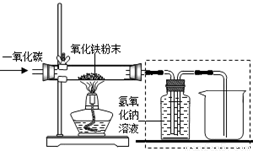
【设计实验】用一氧化碳还原纯净的氧化铁粉末,实验装置如下图。
【进行实验】该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
【分析与讨论】本实验中,玻璃管内固体粉末由红色全部变为黑色。小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料。
【查阅资料】①CO还原Fe2O3的固体产物的成分与反应温度、反应时间等因素有关;
②CO还原Fe2O3的实验过程中固体产物可能有Fe3O4、FeO、Fe;
③NaOH溶液与石灰水相似,能吸收CO2,但不变浑。
④
|
物质性质 |
四氧化三铁 |
氧化亚铁 |
氧化铁 |
铁粉 |
|
颜色 |
黑色 |
黑色 |
红色 |
黑色 |
|
能否被磁铁吸引 |
能 |
不能 |
不能 |
能 |
【实验与猜想】
(1)该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和 。
(2)进行猜想:黑色固体粉末可能a.全部为铁、 b. 、c. 。
【得出结论】
(3)通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称) 。
【反思与评价】
(4)一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度。
(5)实验装置图中采用虚线框内的装置,其作用有 。
A.收集CO B.吸收CO2 C.检验CO2
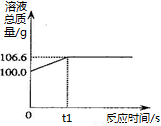
【实践应用】小明和他的同学想测定某赤铁矿石中Fe2O3的质量分数。用CO与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用足量的NaOH溶液完全吸收,该溶液总质量与反应时间的变化关系如右图。
(6)上述反应产生CO2的质量为 g;
(7)计算该赤铁矿石中氧化铁的质量分数。 。(需要有计算过程)
某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究。
 |
【设计实验】用一氧化碳还原纯净的氧化铁粉末,实验装置如下图。
【进行实验】该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
【分析与讨论】本实验中,玻璃管内固体粉末由红色全部变为黑色。小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料。
【查阅资料】①CO还原Fe2O3的固体产物的成分与反应温度、反应时间等因素有关;
②CO还原Fe2O3的实验过程中固体产物可能有Fe3O4、FeO、Fe;
③NaOH溶液与石灰水相似,能吸收CO2,但不变浑。
| 物质性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
④
【实验与猜想】
(1)该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和 ▲ 。
(2)进行猜想:黑色固体粉末可能a.全部为铁、 b. ▲ 、c. ▲ 。
【得出结论】
(3)通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称) ▲ 。
【反思与评价】
(4)一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度。
(5)实验装置图中采用虚线框内的装置,其作用有 ▲ 。
A.收集CO B.吸收CO2 C.检验CO2
【实践应用】小明和他的同学 想测定某赤铁矿石中Fe2O3的质量分数。用CO与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用足量的NaOH溶液完全吸收,该溶液总质量与反应时间的变化关系如右图。
想测定某赤铁矿石中Fe2O3的质量分数。用CO与10g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用足量的NaOH溶液完全吸收,该溶液总质量与反应时间的变化关系如右图。
(6)上述反应产生CO2的质量为 ▲ g;
(7)计算该赤铁矿石中氧化铁的质量分数。 ▲ 。(需要有计算过程)