题目内容
20、氧化物A溶于水生成溶液B,将B溶液分作俩份做实验,实验步骤和现象如下所示:
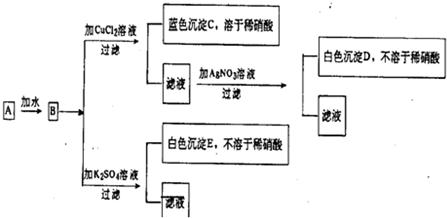
(1)写出C-E的化学式:
C:
(2)写出下列反应的化学方程式:
①B→C:
②B→E:

(1)写出C-E的化学式:
C:
Cu(OH)2
D:AgCl
E:BaSO4
(2)写出下列反应的化学方程式:
①B→C:
Ba(OH)2+CuCl2=BaCl2+Cu(OH)2↓
②B→E:
Ba(OH)2+K2SO4=BaSO4↓+2KOH
分析:蓝色沉淀为氢氧化铜,根据复分解反应相互成分的特点,可判断物质B的溶液中含有OH-;
不溶于稀硝酸的白色沉淀E为硫酸钡或氯化银,根据复分解反应的特点,沉淀E由溶液B与K2SO4反应生成,因此判断白色沉淀E为硫酸钡,同时可得到溶液B中含有Ba2+的结论;
溶液B的确定使得转化关系图中的其它物质可以做出明确的判断.
不溶于稀硝酸的白色沉淀E为硫酸钡或氯化银,根据复分解反应的特点,沉淀E由溶液B与K2SO4反应生成,因此判断白色沉淀E为硫酸钡,同时可得到溶液B中含有Ba2+的结论;
溶液B的确定使得转化关系图中的其它物质可以做出明确的判断.
解答:解:(1)根据沉淀C为蓝色可推断沉淀为氢氧化铜;不溶于稀硝酸的白色沉淀D由硝酸银转化而来,故可推断沉淀D为氯化银;不溶于稀硝酸的白色沉淀E由溶液B与K2SO4反应生成,故可推断沉淀E为硫酸钡;
故答案为:Cu(OH)2;AgCl;BaSO4;
(2)①由溶液B与氯化铜反应生成氢氧化铜蓝色沉淀,溶液B中含OH-;由溶液B与硫酸钾反应生成硫酸钡沉淀,溶液B中含Ba2+;综上所述,溶液B为氢氧化钡溶液;氢氧化钡与氯化铜发生复分解反应,交换成分后生成氢氧化铜和氯化钡;
故答案为:Ba(OH)2+CuCl2=Cu(OH)2↓+BaCl2;
②溶液B为氢氧化钡溶液,与硫酸钾溶液混合通过交换成分,生成不溶于稀硝酸的白色沉淀硫酸钡和氢氧化钾;
故答案为:Ba(OH)2+K2SO4=BaSO4↓+2KOH.
故答案为:Cu(OH)2;AgCl;BaSO4;
(2)①由溶液B与氯化铜反应生成氢氧化铜蓝色沉淀,溶液B中含OH-;由溶液B与硫酸钾反应生成硫酸钡沉淀,溶液B中含Ba2+;综上所述,溶液B为氢氧化钡溶液;氢氧化钡与氯化铜发生复分解反应,交换成分后生成氢氧化铜和氯化钡;
故答案为:Ba(OH)2+CuCl2=Cu(OH)2↓+BaCl2;
②溶液B为氢氧化钡溶液,与硫酸钾溶液混合通过交换成分,生成不溶于稀硝酸的白色沉淀硫酸钡和氢氧化钾;
故答案为:Ba(OH)2+K2SO4=BaSO4↓+2KOH.
点评:利用复分解反应相互交换成分的特点,根据生成的特殊沉淀判断反应物溶液中的离子,从而确定物质为本题的关键.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
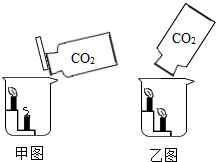 化学兴趣小组的同学对碳及碳的氧化物进行了一系列拓展性探究学习.
化学兴趣小组的同学对碳及碳的氧化物进行了一系列拓展性探究学习.