题目内容
现有一包久置的碱石灰干燥剂(主要成分CaO和NaOH),同学们用它进行了如下探究活动.
【猜想与假设】该干燥剂如果发生变质,则产物可能有 (填一种).
【实验与观察】
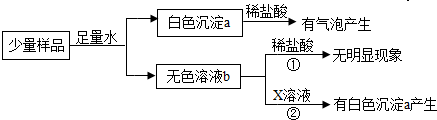
【解释与结论】白色沉淀a为 ,证明该干燥剂已经变质.由反应①可知b溶液中一定没有 ,反应②的化学方程式 ,b溶液中含有的溶质是 .
【猜想与假设】该干燥剂如果发生变质,则产物可能有
【实验与观察】

【解释与结论】白色沉淀a为
考点:药品是否变质的探究,生石灰的性质与用途,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:[猜想与假设]根据CaO和NaOH作用及与空气中的二氧化碳反应的产物分析;
[解释与结论]根据现象分析物质的种类并写出反应的方程式;
[解释与结论]根据现象分析物质的种类并写出反应的方程式;
解答:解:[猜想与假设]因为氧化钙易吸收水分变成氢氧化钙,若继续吸收二氧化碳则变成碳酸钙;氢氧化钠易吸收二氧化碳生成碳酸钠;
故产物可能有:Ca(OH)2(或CaCO3或Na2CO3);
[解释与结论]因为加水不溶解的物质是碳酸钙,故a是碳酸钙;因为反应①加稀盐酸没有明显现象,故一定没有碳酸钠;反应②中若产生白色沉淀,与钙离子有关,所以是氢氧化钙与可溶性的碳酸盐反应产生碳酸钙沉淀,故可以是:Ca(OH)2+Na2CO3═CaCO3+2NaOH;b溶液中含有的溶质是没有变质的氢氧化钠和生成的氢氧化钙;
故答案为:CaCO3;Na2CO3;Ca(OH)2+Na2CO3═CaCO3+2NaOH;NaOH和Ca(OH)2.
故产物可能有:Ca(OH)2(或CaCO3或Na2CO3);
[解释与结论]因为加水不溶解的物质是碳酸钙,故a是碳酸钙;因为反应①加稀盐酸没有明显现象,故一定没有碳酸钠;反应②中若产生白色沉淀,与钙离子有关,所以是氢氧化钙与可溶性的碳酸盐反应产生碳酸钙沉淀,故可以是:Ca(OH)2+Na2CO3═CaCO3+2NaOH;b溶液中含有的溶质是没有变质的氢氧化钠和生成的氢氧化钙;
故答案为:CaCO3;Na2CO3;Ca(OH)2+Na2CO3═CaCO3+2NaOH;NaOH和Ca(OH)2.
点评:实验设计和猜想都要根据物质相应的性质来实施,所以应熟悉物质的性质.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
下列各组物质中的两种物质不能用同一化学式表示的是( )
| A、食盐、氯化钠 |
| B、苛性钠、烧碱 |
| C、胆矾、硫酸铜 |
| D、熟石灰、消石灰 |
在配制100g溶质质量分数为10%的蔗糖溶液时,导致溶液中蔗糖的质量分数偏小的可能原因有( )
| A、用量筒量取水时俯视读数 |
| B、用来配制溶液的烧杯刚刚用少量蒸馏水润洗过 |
| C、用托盘天平称取蔗糖时,将蔗糖放在右盘,称量时没有使用游码 |
| D、在把量好的水倒入烧杯时,有少量水溅出烧杯 |
下列有关酸、碱、盐的生产或应用的说法不合理的是( )
| A、将草木灰(含K2CO3)与氯化铵混合施用 |
| B、粗盐可通过重结晶和加物质纯化后变为精盐 |
| C、用石灰乳与硫酸铜溶液混合配制防治植物病害的波尔多液 |
| D、汽车或电动车的蓄电池中用到的硫酸溶液是由浓硫酸稀释而成 |
 化学源于生活,生活中蕴含着许多化学知识.
化学源于生活,生活中蕴含着许多化学知识.

 A、B、C、D四种物质的转化关系如图(所需反应条件略去)
A、B、C、D四种物质的转化关系如图(所需反应条件略去)