题目内容
14.我国首台使用二甲醚为燃料的城市客车有效地解决了公交车冒黑烟的问题,已知二甲醚的化学式为C2H6O.(1)二甲醚分子中碳原子、氧原子和氢原子的原子个数比为:2:6:1.
(2)计算C2H6O中碳元素的质量分数(保留一位小数).
分析 (1)根据1个二甲醚分子的构成,进行分析解答.
(2)根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
解答 解:(1)一个二甲醚分子是由2个碳原子、6个氢原子和1个氧原子构成的,则二甲醚分子中碳原子、氧原子和氢原子的原子个数比为2:6:1.
(2)C2H6O中碳元素的质量分数为$\frac{12×2}{12×2+1×6+16}$×100%≈52.2%.
故答案为:(1)2:6:1;(2)52.2%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
4.有关下列实验的说法中,不合理的是( )
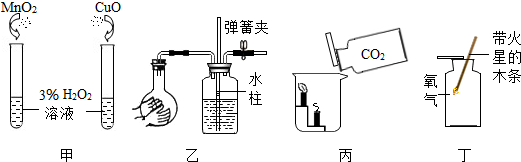

| A. | 甲实验中左试管比右试管放出气泡快,说明MnO2比CuO的催化效果好 | |
| B. | 乙实验中装置中玻璃导管内水柱上升,说明此装置气密性良好 | |
| C. | 丙实验中低的蜡烛先熄灭,说明CO2的密度大于空气 | |
| D. | 丁实验中带火星的木条复燃,说明集气瓶中氧气已收集满 |
5.下列化学现象的描述,正确的是( )
| A. | 红磷在空气中燃烧,产生大量的白雾 | |
| B. | 铁丝在空气中燃烧,火星四射,生成白色固体 | |
| C. | 木炭在氧气中燃烧,发出白光,并放出热量 | |
| D. | 硫在空气中燃烧发出明亮的蓝紫色的火焰 |
9.下列关于生活常识的说法中正确的是( )
| A. | 用肥皂水区别软水和硬水 | |
| B. | 天然果汁中不含任何化学物质 | |
| C. | 绿色食品就是指颜色一定为绿色的食品 | |
| D. | 白色污染是指白色粉尘造成的污染 |
19.鉴别空气、O2、CO2三瓶气体的方法是( )
| A. | 闻气味 | B. | 分别插入燃着的木条 | ||
| C. | 观察颜色 | D. | 分别倒入少量澄清石灰水,振荡 |
5.已知磷酸二氢铵(NH4H2PO4)是一种经常使用的化肥,下列说法正确的是( )
| A. | 磷酸二氢铵是一种复合肥料 | |
| B. | 磷酸二氢铵是由氮、氢、磷、氧四种原子构成 | |
| C. | 磷酸二氢铵中氮、氢、磷、氧元素的质量比为1:6:1:4 | |
| D. | 磷酸二氢铵还可以与碳酸钾混合使用,从而土壤中的氮、钾、磷元素含量均增多了 |