题目内容
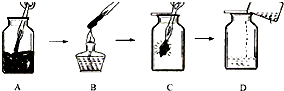 如图是进行“高锰酸钾制取氧气和氧气性质”的探究,请完成下列探究内容:
如图是进行“高锰酸钾制取氧气和氧气性质”的探究,请完成下列探究内容:(1)制取并收集两瓶氧气时,我用了集气瓶、玻璃片、试管、铁架台(带铁夹)、导管、橡皮塞、水槽、药匙、火柴、
(2)氧气收集完成后,停止加热时,我是先
(3)做氧气的性质探究时,我用了如图所示的操作流程.本流程我探究的内容是
(4)D操作用烧杯倾倒的液体是
考点:氧气的制取装置,氧气的化学性质,氧气的收集方法,制取氧气的操作步骤和注意点,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.进行“高锰酸钾制取氧气和氧气性质”的探究时,用到的仪器和药品有:集气瓶、玻璃片、试管、铁架台(带铁夹)、导管、橡皮塞、水槽、药匙、火柴、酒精灯、棉花团、高锰酸钾等;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂.做氧气的性质探究时,我用了如图所示的操作流程.本流程我探究的内容是:探究木炭在氧气中燃烧,C操作,为了使木炭,与氧气完全反应,我的操作方法是由上到下慢慢进入;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;得出的探究结论是:木炭在氧气反应更剧烈,生成物是二氧化碳.
解答:解:(1)进行“高锰酸钾制取氧气和氧气性质”的探究时,用到的仪器和药品有:集气瓶、玻璃片、试管、铁架台(带铁夹)、导管、橡皮塞、水槽、药匙、火柴、酒精灯、棉花团、高锰酸钾等;故答案为:酒精灯;棉花团;高锰酸钾;
(2)实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;故答案为:移出导管;熄灭酒精灯;
(3)做氧气的性质探究时,我用了如图所示的操作流程.本流程我探究的内容是:探究木炭在氧气中燃烧,C操作,为了使木炭,与氧气完全反应,我的操作方法是由上到下慢慢进入;故答案为:探究木炭在氧气中燃烧;木炭;由上到下慢慢进入;
(4)二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;得出的探究结论是:木炭在氧气反应更剧烈,生成物是二氧化碳;故答案为:澄清的石灰水;木炭在氧气反应更剧烈,生成物是二氧化碳;
(2)实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;故答案为:移出导管;熄灭酒精灯;
(3)做氧气的性质探究时,我用了如图所示的操作流程.本流程我探究的内容是:探究木炭在氧气中燃烧,C操作,为了使木炭,与氧气完全反应,我的操作方法是由上到下慢慢进入;故答案为:探究木炭在氧气中燃烧;木炭;由上到下慢慢进入;
(4)二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;得出的探究结论是:木炭在氧气反应更剧烈,生成物是二氧化碳;故答案为:澄清的石灰水;木炭在氧气反应更剧烈,生成物是二氧化碳;
点评:本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了氧气的性质和二氧化碳的检验等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
在化学符号2H、2Fe2+、2H2、2Cu、2H2O 中,数字“2”表示的意义不尽相同,其中“2”的意义用来表示分子个数的有( )
| A、1个 | B、2个 | C、3个 | D、4个 |


 空气是一种重要资源,空气质量成为人们日益关注的话题.
空气是一种重要资源,空气质量成为人们日益关注的话题.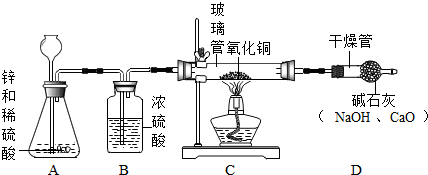
 实验室中可用如图装置分离CO和CO2的混合气体:
实验室中可用如图装置分离CO和CO2的混合气体: 电解水实验:负极产生的是
电解水实验:负极产生的是