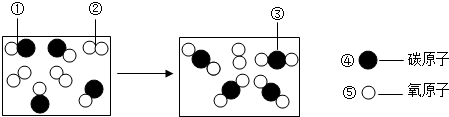
题目内容
某白色固体是CuSO4、CaCO3、Ba(NO3)2、Na2SO4、NaOH中的一种或几种,为确定其组成,同学们进行了如图实验.

(1)原固体中一定没有 .
(2)实验过程中产生气体的化学方程式为 .
(3)无色溶液B中的溶质是
(4)要确定原固体中可能存在的物质,还需要进行的实验是 .

(1)原固体中一定没有
(2)实验过程中产生气体的化学方程式为
(3)无色溶液B中的溶质是
(4)要确定原固体中可能存在的物质,还需要进行的实验是
考点:物质的鉴别、推断,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:混合物组成的推断题
分析:根据硫酸铜溶液为蓝色,所以原白色固体加足量水溶解,得到白色固体和无色溶液,说明一定没有硫酸铜;硫酸钡沉淀不溶于水稀硝酸,而碳酸钙沉淀能和硝酸反应生成二氧化碳气体,所以加入过量稀硝酸后,还有白色固体,说明固体为硫酸钡,硫酸钡是由硝酸钡和硫酸钠溶液反应生成的,有无色气体生成说明一定含有碳酸钙沉淀进行解答.
解答:解:(1)硫酸铜溶液为蓝色,所以原白色固体加足量水溶解,得到白色固体和无色溶液,说明一定没有硫酸铜;
(2)硫酸钡沉淀不溶于水稀硝酸,而碳酸钙沉淀能和硝酸反应生成硝酸钙、水和二氧化碳气体,化学方程式为CaCO3+2HNO3═Ca(NO3)2+H2O+CO2↑;
(3)硫酸钡沉淀不溶于水稀硝酸,而碳酸钙沉淀能和硝酸反应生成硝酸钙、水和二氧化碳气体,所以加入过量稀硝酸后,无色溶液B中的溶质是硝酸钙和硝酸;
(4)硫酸铜溶液为蓝色,所以原白色固体加足量水溶解,得到白色固体和无色溶液,说明一定没有硫酸铜;硫酸钡沉淀不溶于水稀硝酸,而碳酸钙沉淀能和硝酸反应生成二氧化碳气体,所以加入过量稀硝酸后,还有白色固体,说明固体为硫酸钡,硫酸钡是由硝酸钡和硫酸钠溶液反应生成的,有无色气体生成说明一定含有碳酸钙沉淀,同时还含有硫酸钠和硝酸钡,但是不能确定是否含有氢氧化钠,氢氧化钠溶于水显碱性,能使酚酞试液变红,所以要确定原固体中可能存在的物质,需要进行的实验是取少量无色溶液A,滴加无色酚酞,变红色则有氢氧化钠.
故答案为:(1)CuSO4;(2)CaCO3+2HNO3═Ca(NO3)2+H2O+CO2↑
(3)Ca(NO3)2、HNO3;
(4)取少量无色溶液A,滴加无色酚酞,变红色则有氢氧化钠.
(2)硫酸钡沉淀不溶于水稀硝酸,而碳酸钙沉淀能和硝酸反应生成硝酸钙、水和二氧化碳气体,化学方程式为CaCO3+2HNO3═Ca(NO3)2+H2O+CO2↑;
(3)硫酸钡沉淀不溶于水稀硝酸,而碳酸钙沉淀能和硝酸反应生成硝酸钙、水和二氧化碳气体,所以加入过量稀硝酸后,无色溶液B中的溶质是硝酸钙和硝酸;
(4)硫酸铜溶液为蓝色,所以原白色固体加足量水溶解,得到白色固体和无色溶液,说明一定没有硫酸铜;硫酸钡沉淀不溶于水稀硝酸,而碳酸钙沉淀能和硝酸反应生成二氧化碳气体,所以加入过量稀硝酸后,还有白色固体,说明固体为硫酸钡,硫酸钡是由硝酸钡和硫酸钠溶液反应生成的,有无色气体生成说明一定含有碳酸钙沉淀,同时还含有硫酸钠和硝酸钡,但是不能确定是否含有氢氧化钠,氢氧化钠溶于水显碱性,能使酚酞试液变红,所以要确定原固体中可能存在的物质,需要进行的实验是取少量无色溶液A,滴加无色酚酞,变红色则有氢氧化钠.
故答案为:(1)CuSO4;(2)CaCO3+2HNO3═Ca(NO3)2+H2O+CO2↑
(3)Ca(NO3)2、HNO3;
(4)取少量无色溶液A,滴加无色酚酞,变红色则有氢氧化钠.
点评:本题考查了混合物组成的推断,完成此题,可以结合题干提供的实验现象根据物质的性质进行.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
物质的化学式与俗名对应正确的是( )
| A、CaO:石灰石 |
| B、CuSO4:胆矾 |
| C、Na2CO3?10H2O:纯碱 |
| D、Ca(OH)2:熟石灰 |
 化学兴趣小组设计的创新实验是“火龙生字”.在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1).用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(见图2).在场的同学对此产生了浓厚的兴趣,并进行了如下研究:
化学兴趣小组设计的创新实验是“火龙生字”.在成果展示现场,某同学用硝酸钾的热饱和溶液先在白纸上书写“火”字,晾干后白纸上出现硝酸钾晶体(见图1).用带火星的木条接触硝酸钾晶体,就会观察到白纸上写过字的地方燃烧并迅速蔓延,留下“火”字的黑色痕迹(见图2).在场的同学对此产生了浓厚的兴趣,并进行了如下研究:

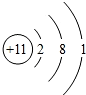 是某粒子的结构示意图,该粒子在化学反应中容易
是某粒子的结构示意图,该粒子在化学反应中容易