题目内容
样品11 g放入烧杯中,再加入 50 g稀盐酸,恰好完全反应,称得烧杯中的溶液质量为56.6 g。(已知:Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑)
50 g稀盐酸,恰好完全反应,称得烧杯中的溶液质量为56.6 g。(已知:Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑)
请计算:
(1)碳酸钠样品中碳酸钠的质量分数(保留一位小数)。
(2)反应后所得溶液中溶质的质量。
【解】生成二氧化碳的质量为:11 g + 50 g - 56.6 g = 4.4 g
设:样品中碳酸钠的质量为x,生成氯化钠的质量为y。
Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
106 117 44
x y 4.4 g


x = 10.6 g y = 11.7 g
|

|
答:样品中碳酸钠的质量分数为96.4%。所得溶液中氯化钠的质量为12.1 g。

练习册系列答案
相关题目
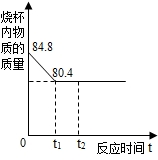 工业上用侯氏制碱法制得的纯碱样品中含有一定量的氯化钠.现称取只含有氯化钠杂质的纯碱样品11.8g放入盛73g稀盐酸的烧杯中,恰好完全反应.反应过程中烧杯内物质的质量随时间的变化关系如图所示.试回答下列问题:
工业上用侯氏制碱法制得的纯碱样品中含有一定量的氯化钠.现称取只含有氯化钠杂质的纯碱样品11.8g放入盛73g稀盐酸的烧杯中,恰好完全反应.反应过程中烧杯内物质的质量随时间的变化关系如图所示.试回答下列问题: 工业上用侯氏制碱法制得的纯碱样品中含有一定量的氯化钠.现称取只含有氯化钠杂质的纯碱样品11.8g放入盛73g稀盐酸的烧杯中,恰好完全反应.反应过程中烧杯内物质的质量随时间的变化关系如图所示.试回答下列问题:
工业上用侯氏制碱法制得的纯碱样品中含有一定量的氯化钠.现称取只含有氯化钠杂质的纯碱样品11.8g放入盛73g稀盐酸的烧杯中,恰好完全反应.反应过程中烧杯内物质的质量随时间的变化关系如图所示.试回答下列问题: 工业上用侯氏制碱法制得的纯碱样品中含有一定量的氯化钠.现称取只含有氯化钠杂质的纯碱样品11.8g放入盛73g稀盐酸的烧杯中,恰好完全反应.反应过程中烧杯内物质的质量随时间的变化关系如图所示.试回答下列问题:
工业上用侯氏制碱法制得的纯碱样品中含有一定量的氯化钠.现称取只含有氯化钠杂质的纯碱样品11.8g放入盛73g稀盐酸的烧杯中,恰好完全反应.反应过程中烧杯内物质的质量随时间的变化关系如图所示.试回答下列问题: