题目内容
5. 如图为空气成分示意图(按体积计算),其中“a”代表的是( )
如图为空气成分示意图(按体积计算),其中“a”代表的是( )| A. | 氮气 | B. | 氧气 | C. | 二氧化碳 | D. | 稀有气体 |
分析 空气中各成分的体积分数分别是:氮气大约占78%、氧气大约占21%、稀有气体大约占0.94%、二氧化碳大约占0.03%、水蒸气和其它气体和杂质大约占0.03%;空气中氮气的体积分数最大,因此“a”代表的是氮气.
解答 解:A、氮气大约占空气体积的78%,空气中氮气的体积分数最大,因此“a”代表的是氮气,故选项正确;
B、氧气大约占空气体积的21%,故选项错误;
C、二氧化碳大约占空气体积的0.03%,故选项错误;
D、稀有气体大约占空气体积的0.94%,故选项错误;
故选A
点评 本考点考查了空气中各种气体的含量,同学们要加强记忆有关的知识点,在理解的基础上加以应用,本考点基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
相关题目
15.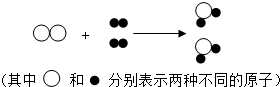 如图,表示在一定条件下发生的某化学反应,则下列说法正确的是( )
如图,表示在一定条件下发生的某化学反应,则下列说法正确的是( )
 如图,表示在一定条件下发生的某化学反应,则下列说法正确的是( )
如图,表示在一定条件下发生的某化学反应,则下列说法正确的是( )| A. | 两种反应物均为化合物 | B. | 该反应不符合质量守恒定律 | ||
| C. | 该反应前后元素的种类发生了改变 | D. | 该反应属于化合反应 |
20.已知下列反应能够发生:①Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;②Cu+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O;③Cu+Cl2$\frac{\underline{\;\;△\;\;}}{\;}$CuCl2.其中NO2、SO2、Cl2都是有毒气体,请选择用铜制取CuSO4•5H2O晶体最合理的方案是( )
| A. | Cu+Cl2→CuCl2$\stackrel{NaOH}{→}$Cu(OH)2$\stackrel{H_{2}SO_{4}}{→}$CuSO4溶液→蒸发浓缩→冷却结晶→过滤 | |
| B. | Cu+HNO3(浓)→Cu(NO3)2 $\stackrel{NaOH}{→}$Cu(OH)2$\stackrel{浓H_{2}SO_{4}}{→}$CuSO4浓溶液→冷却结晶→过滤 | |
| C. | Cu+O2→CuO$\stackrel{H_{2}SO_{4}}{→}$ CuSO4溶液→蒸发浓缩→冷却结晶→过滤洗涤 | |
| D. | Cu+H2SO4(浓)→CuSO4浓溶液→冷却结晶→过滤洗涤 |
14.下列各组仪器,常用于物质分离的是( )
①漏斗 ②容量瓶 ③温度计 ④分液漏斗 ⑤天平
⑥量筒 ⑦胶头滴管 ⑧蒸馏烧瓶 ⑨集气瓶.
①漏斗 ②容量瓶 ③温度计 ④分液漏斗 ⑤天平
⑥量筒 ⑦胶头滴管 ⑧蒸馏烧瓶 ⑨集气瓶.
| A. | ①④⑧ | B. | ②⑥⑦⑨ | C. | ①③⑦ | D. | ④⑤⑥⑧ |
4.在过氧化氢溶液的分解反应中,二氧化锰能作催化剂.下列有关催化剂的说法正确的是D(选填序号)
A.在化学反应后其质量减小 B.在化学反应后其化学性质发生了变化
C.能增大生成物的质量 D.能改变化学反应速率
【提出问题】在过氧化氢溶液的分解反应中,除了二氧化锰,能否有其他物质也能作催化剂?
【查阅资料】在过氧化氢溶液的分解反应中,氧化铜也能作为催化剂
【进行实验】用天平称量0.2g氧化铜,取5mL5%过氧化氢溶液于试管中,进行如下实验:

(1)填写表
(2)步骤①的目的是与步骤③对比,检验加入氧化铜前后过氧化氢溶液的分解速率有无变化
(3)步骤④对应的实验操作是过滤,需用到的玻璃仪器有烧杯、玻璃棒、漏斗
【拓展探究】设计如下四组实验,比较二氧化锰和氧化铜对过氧化氢溶液分解的催化作用,其中观察效果最差的C
A.第一组同时实验,观察比较反应过程中两个气球体积的变化
B.第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢
C.第三组分两次实验,看木条是否能复燃
D.第四组分两次实验,比较收集一定体积的气体所需要的时间.
A.在化学反应后其质量减小 B.在化学反应后其化学性质发生了变化
C.能增大生成物的质量 D.能改变化学反应速率
【提出问题】在过氧化氢溶液的分解反应中,除了二氧化锰,能否有其他物质也能作催化剂?
【查阅资料】在过氧化氢溶液的分解反应中,氧化铜也能作为催化剂
【进行实验】用天平称量0.2g氧化铜,取5mL5%过氧化氢溶液于试管中,进行如下实验:

(1)填写表
| 步骤③现象 | 步骤⑥现象 | 步骤⑦现象 | 结论 |
| 剧烈反应 有气泡产生 带火星的木条复燃 | 称量的氧化铜的质量仍为0.2g | 溶液中有气泡放出 带火星的木条复燃 | 在过氧化氢溶液的分解反应中,氧化铜也能作催化剂 |
(3)步骤④对应的实验操作是过滤,需用到的玻璃仪器有烧杯、玻璃棒、漏斗
【拓展探究】设计如下四组实验,比较二氧化锰和氧化铜对过氧化氢溶液分解的催化作用,其中观察效果最差的C
 |  |  |  |
| 第一组 | 第二组 | 第三组 | 第四组 |
B.第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢
C.第三组分两次实验,看木条是否能复燃
D.第四组分两次实验,比较收集一定体积的气体所需要的时间.