题目内容
小明欲测定某发酵粉中小苏打的含量(假设发酵粉中其它成分不反应也不溶于水).请回答下列问题:
(1)配制100g的质量分数为7.3%的稀盐酸,需36.5%的浓盐酸的质量是 ;
(2)取10g发酵粉放入烧杯中,向其中滴加50g上述稀盐酸时恰好不再产生气泡,测得杯中的混合物质量为55.6g.
①写出上述反应的化学反应方程式 ;
②写出求解发酵粉中小苏打质量(X)的比例式 ;
③发酵粉中小苏打的质量分数为 ;
④过滤后,将所得滤液蒸发掉4g水后,所得溶液仍为不饱和溶液,则所得溶液中溶质的质量分数为 .
(1)配制100g的质量分数为7.3%的稀盐酸,需36.5%的浓盐酸的质量是
(2)取10g发酵粉放入烧杯中,向其中滴加50g上述稀盐酸时恰好不再产生气泡,测得杯中的混合物质量为55.6g.
①写出上述反应的化学反应方程式
②写出求解发酵粉中小苏打质量(X)的比例式
③发酵粉中小苏打的质量分数为
④过滤后,将所得滤液蒸发掉4g水后,所得溶液仍为不饱和溶液,则所得溶液中溶质的质量分数为
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)稀释问题不变来解答;
(2)可以根据质量守恒定律书写化学方程式,根据化学方程式求某些物质的质量,根据质量分数的含义求溶液中溶质的质量分数.
(2)可以根据质量守恒定律书写化学方程式,根据化学方程式求某些物质的质量,根据质量分数的含义求溶液中溶质的质量分数.
解答:解:(1)设需36.5%的浓盐酸的质量为x
100g×7.3%=x×36.5%
x=20g
(2)①碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑
②反应生成的二氧化碳的质量为:10g+50g-55.6g=4.4g
设小苏打的质量为X,生成的氯化钠的质量为Y.
NaHCO3+HCl═NaCl+H2O+CO2↑
84 58.5 44
X Y 4.4g
=
;
=
X=8.4g; y=5.85g
③发酵粉中小苏打的质量分数为:
×100%=84%;
④所得溶液中溶质的质量分数为:
×100%=11.7%.
答案:(1)20g;
(2)①NaHCO3+HCl═NaCl+H2O+CO2↑;
②
=
;
③84%;
④11.7%.
100g×7.3%=x×36.5%
x=20g
(2)①碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑
②反应生成的二氧化碳的质量为:10g+50g-55.6g=4.4g
设小苏打的质量为X,生成的氯化钠的质量为Y.
NaHCO3+HCl═NaCl+H2O+CO2↑
84 58.5 44
X Y 4.4g
| 84 |
| X |
| 44 |
| 4.4g |
| 58.5 |
| y |
| 44 |
| 4.4g |
X=8.4g; y=5.85g
③发酵粉中小苏打的质量分数为:
| 8.4g |
| 10g |
④所得溶液中溶质的质量分数为:
| 5.85g |
| 8.4g+50g-4.4g-4g |
答案:(1)20g;
(2)①NaHCO3+HCl═NaCl+H2O+CO2↑;
②
| 84 |
| X |
| 44 |
| 4.4g |
③84%;
④11.7%.
点评:本题主要考查了化学方程式的书写及其根据化学方程式进行相关计算等方面的问题.

练习册系列答案
相关题目
下列变化,属于化学变化的是( )
| A、天热吃雪糕时,发现雪糕慢慢熔化 |
| B、洗净的铁锅常会出现锈迹 |
| C、潮湿的衣服在空气中放置会晾干 |
| D、夏天从冰箱取出的瓶子外壁迅速附着一层水 |




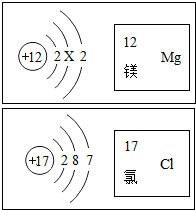 如图是镁和氯两种元素的有关信息,请回答下列问题:
如图是镁和氯两种元素的有关信息,请回答下列问题: 一种石灰石样品的成分是CaCO3和SiO2.为了测定该样品中CaCO3的质量分数,现将100g盐酸等分5次加到35g此样品中,得到部分数据与图象.
一种石灰石样品的成分是CaCO3和SiO2.为了测定该样品中CaCO3的质量分数,现将100g盐酸等分5次加到35g此样品中,得到部分数据与图象.