题目内容
11.2g硫粉放在一定质量的氧气中燃烧,有关实验数据如表中所示:| 第一次 | 第二次 | 第三次 | |
| O2的质量(g) | 1.5 | 2 | 3 |
| SO2的质量(g) | 3 |
(2)第二次实验中,生成SO2的质量为4g.
(3)下列关于三次实验生成的SO2的质量大小比较正确的是CD(选填字母编号).
A.第三次实验生成的SO2质量最大
B.三次实验生成物SO2的质量都是3g
C.第二次与第三次实验生成的SO2质量相等
D.第二次与第三次实验生成的SO2比第一次实验生成的SO2质量大.
分析 (1)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.由图表数据可知,第一次参加反应的S的质量=生成的SO2的质量-O2的质量,然后据此计算出三种物质的质量比;
(2)根据硫与氧气反应的化学方程式和参与反应的氧气的质量,即可计算出第二次实验生成二氧化硫的质量;
(3)根据质量守恒定律和(2)中计算出的第二次实验生成二氧化硫的质量,即可计算出第二次反应中参与反应的S的质量为4g,说明,此时硫已完全反应,故第三次生成的二氧化硫的质量为8g.
解答 解:(1)第一次参加反应的S的质量=3g-1.5g=1.5g;
∴第一次实验中,参加反应的S、O2、生成的SO2三种物质的质量比为:1.5g:1.5g:3g=1:1:2;
(2)设第二次实验生成二氧化硫的质量为y,
S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2
32 64
2g y
$\frac{32}{2g}=\frac{64}{y}$
y=4g
(3)因为第二次反应中参与反应的S的质量为2g,说明,此时硫已完全反应,故第三次生成的二氧化硫的质量为4g.
故第二次与第三次实验生成的SO2质量相等,第二次与第三次实验生成的SO2比第一次实验生成的SO2质量大.
答案:
(1)1:1:2;
(2)4;
(3)CD.
点评 本题主要考查学生运用化学方程式和质量守恒定律综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
4.CO和CO2对人体健康有着重要的影响.关于一氧化碳和二氧化碳的叙述中,合理的是( )
| A. | 都是无色有毒的气体 | |
| B. | 都是氧化物,都能与氢氧化钙溶液反应 | |
| C. | 都能用碳和氧气反应制得 | |
| D. | 都能溶于水生成碳酸 |
2.生活中的如图物质属于纯净物的是( )
| A. |  食品袋内防腐的氨气 | B. |  食醋 | ||
| C. |  碳酸饮料 | D. |  矿泉水 |
3.目前,科学家提出了一种最经济最理想的获得氢能源的循环体系,如图所示.下列说法正确的是( )


| A. | 在此循环中发生了反应:2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑ | |
| B. | 燃料电池能够使化学反应产生的能量转化为电能 | |
| C. | 该氢能源的循环体系能够实现电能和太阳能的相互转化 | |
| D. | 目前未能使用氢气作为普通燃料的主要原因是氢气易爆炸 |
20.洗涤是生产、生活及实验室中常见操作,下列有关洗涤方法不正确的是( )
| A. | 汽车修理工用汽油洗涤手上的油污 | |
| B. | 做完碘升华实验后的试管,用酒精清洗 | |
| C. | 沾有油污的炉具,用含有氢氧化钠的清洁剂清洗 | |
| D. | 用钢丝球擦洗铝锅表面的污垢 |
 海洋是地球上最大的储水库,浩瀚的海洋蕴含着丰富的化学资源.我市具有较长的海岸线,海洋资源开发前景广阔.
海洋是地球上最大的储水库,浩瀚的海洋蕴含着丰富的化学资源.我市具有较长的海岸线,海洋资源开发前景广阔.
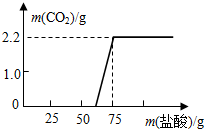 实验室中久置的NaOH会因为吸收空气中的CO2而变质.为了测定实验室中久置的NaOH的变质程度,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,确定样品中NaOH的变质程度.若实验测得加入稀盐酸的质量与产生的CO2气体的质量关系如图所示.请根据图象分析计算:
实验室中久置的NaOH会因为吸收空气中的CO2而变质.为了测定实验室中久置的NaOH的变质程度,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,确定样品中NaOH的变质程度.若实验测得加入稀盐酸的质量与产生的CO2气体的质量关系如图所示.请根据图象分析计算: